공명 구조. resonance structures
기여 구조. contributing structures
---------------------------------------------------
▶ 참고: 제8장 화학 결합의 기본 개념. 목차
[ https://ywpop.tistory.com/15249 ]
▶ 참고: 루이스 구조. Lewis structure
[ https://ywpop.tistory.com/2541 ]
---------------------------------------------------
Once upon a time...
어떤 분자의 루이스 구조를 그려보면(완성하면),
대부분의 경우, 가장 안정한 루이스 구조는
오로지 단 1개뿐이었다.
근데... 가끔씩...
루이스 구조를 그려봤더니...
안정성이 동등한 루이스 구조가
2개 이상 나오는 분자가 있더라...
공명구조 얘기는 여기서부터 시작한다.
공명구조 (resonance structures)
▶ 단 한 개의 Lewis 구조만으로
실제 분자(또는 다원자 이온)를 정확히 나타낼 수 없을 때,
분자가 가지는 2개 이상의 Lewis 구조를 ‘공명구조’라 한다.
A resonance form is another way of drawing
a Lewis dot structure for a given compound.
Equivalent Lewis structures are called resonance forms.
( 2개 이상의 동등한 Lewis 구조 = resonance forms )
▶ 중요한 점
> 분자가 가지는 모든 루이스 구조의 안정성은 동등하다.
( 기여도는 동등하다. )
( 참고: 기여도가 동등하지 않아도 된다는 설명도 있음. )
▶ 공명구조라는 개념이 탄생한 이유
> 어떤 분자의 루이스 구조를 완성해보니,
단 1개의 Lewis 구조식만으로는 나타낼 수 없었다.
안정성이 동동한 구조가 2개 이상 나오더라...
→ 이 때문에 어떤 분자의 실제 구조를
단 1개의 Lewis 구조식만으로는 나타낼 수 없었다.
→ 그렇다고, 아예 구조식으로 안 나타낼 수도 없고...
→ 어떻게든 이와 같은 분자들도 구조식으로 표현은 해야겠다.
→ 그래서 만든 개념이 공명구조이다.
▶ 중요한 점
> 공명구조는 실제로 존재하는 구조가 아니라 ‘가상의 구조’라는 것.
▶ 공명 구조를 갖는 물질(분자 또는 이온)에서
각각의 결합 길이는 모두 같고,
그 결합 길이는 동일 원자간의
단일 결합보다는 길고, 이중 결합보다는 짧다.
그래서 공명 구조를 갖는 물질의 결합을 ‘1.5 결합’이라고도 한다.
[참고] 공명 구조를 판단할 때는
이성질체를 판단할 때처럼 분자를 회전시키지 않는다.
분자 내 모든 원자의 위치가 고정된 상태에서
안정성이 동등한 다른 루이스 구조(결합 구조)가 가능하면,
그것이 공명 구조라고 정의 내렸기 때문이다.
[공명 구조를 그릴 때 원칙]
① 각 원자의 연결 순서(공간 배치 구조)는 동일해야 한다.
> π-전자 (비결합 전자쌍)만 이동 가능.
② 모든 원자는 옥텟 규칙(octet rule)을 만족해야 한다.
> 단, 수소, 헬륨은 제외.
③ 각 구조가 갖는 비결합 전자의 수는 동일해야 한다.
---------------------------------------------------
▶ 분자(또는 다원자 이온)의 결합을
한 개의 Lewis 구조만으로 정확히 나타낼 수 없을 때,
분자가 가지는 2개 이상의 Lewis 구조를
‘공명 구조’ 또는 ‘기여 구조’라 한다.
> 공명 구조는 실제로 존재하는 구조가 아니라 가상의 구조이다.
> 공명 구조를 갖는 물질은
비결합(비공유) 전자쌍이나 다중 결합(π 전자)을 가지고 있다.
⇨ 이들 전자들의 특징: 이웃한 결합(또는 원자)으로 이동할 수 있다.
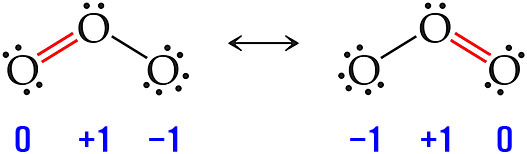
[그림] 오존 분자의 ‘동등한’ 2개 Lewis 구조.
⇨ Lewis 구조 하나만으로, 오존 분자를 정확하게 나타낼 수 없다.
⇨ 오존 분자는 2개 공명 구조(↔ 사용)로 나타낼 수 있다.
( 참고: 오존의 루이스 구조 그리기 https://ywpop.tistory.com/5291 )
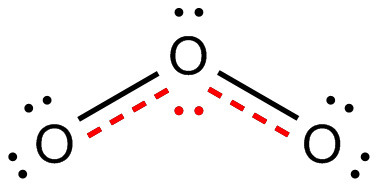
[그림] 오존의 실제 구조. 오존의 공명 혼성(resonance hybrid) 구조.
⇨ O–O 결합 길이는 서로 같다. (1.278 Å)
⇨ 양끝 산소 원자의 전하는 –1/2.
⇨ 오존에서 O–O 결합을 ‘1.5 결합’으로 설명하기도 한다.
( 참고: 벤젠의 공명 혼성 구조 https://ywpop.tistory.com/2035 )
[참고] 산소–산소 원자간 결합 길이
> O–O 단일 결합: 1.48 Å
> O=O 이중 결합: 1.21 Å
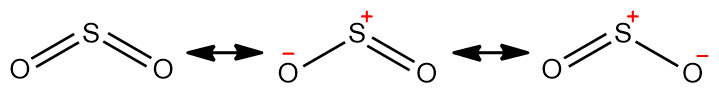
[그림] SO2의 공명 구조. 안정성이 동등하지 않는데도, 공명 구조(?).
( 참고: SO2의 루이스 구조 그리기 https://ywpop.tistory.com/3595 )
[키워드] 공명 구조의 정의 기준, 공명 구조 정의 기준, 공명 구조 기준, 공명 기준, 공명 구조의 정의 사전, 공명 구조 정의 사전, 공명 구조 사전, 공명 사전, 공명 경전, resonance dic
'일반화학 > [08장] 화학결합의 기본 개념' 카테고리의 다른 글
| 격자 에너지. Lattice Energy. NaCl ★ (0) | 2015.01.05 |
|---|---|
| 3가지 화학 결합 ★ (1) | 2014.11.29 |
| NH4^+는 극성 분자인가? 쌍극자모멘트 값은? (1) | 2014.11.04 |
| 루이스 전자 점 기호로 나타낸 주기율표 (1) | 2014.10.13 |
| 팔전자 규칙. 옥텟 규칙. octet rule ★ (3) | 2014.06.26 |
| 일산화탄소(carbon monoxide, CO)의 작은 쌍극자 모멘트(dipole moment) (1) | 2014.06.25 |
| 쌍극자(dipole), 쌍극자모멘트(dipole moment), 분자의 극성 ★ (1) | 2014.06.03 |
| 전기음성도 (electronegativity) ★ (0) | 2014.05.26 |



댓글