왜 정사면체는 쌍극자모멘트가 0인가요?
예를 들어 CH4 같은 경우는 탄소쪽으로 전자쌍이 몰려있는데도
왜 쌍극자모멘트가 0인가요?
---------------------------------------------------
▶ 참고: 쌍극자 모멘트
[ https://ywpop.tistory.com/2581 ]
---------------------------------------------------
왜냐하면 결합의 쌍극자 모멘트는
크기와 방향, 둘 다 가진 벡터량이고,
한 물질의 쌍극자 모멘트는
각 결합의 벡터량을 모두 합한 벡터합이기 때문입니다.
예를 들어, 똑같은 힘을 가진 4사람이
동서남북으로 줄다리기 시합을 하면
어느 쪽으로도 움직이지 않고,
똑같은 힘을 가진 4사람이
가운데에 공을 놓고 동서남북에서 밀면
공은 어느 쪽으로도 움직이지 않습니다.
CH4도 이와 같기 때문에
알짜 전하가 발생하지 않습니다.
이 때문에 쌍극자 모멘트가 0입니다.


[그림] Molecular geometry of CH4.
---------------------------------------------------
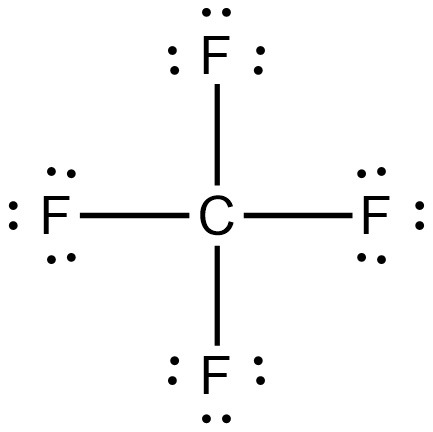

[그림] Lewis structure of CF4 and molecular geometry of CF4.
---------------------------------------------------
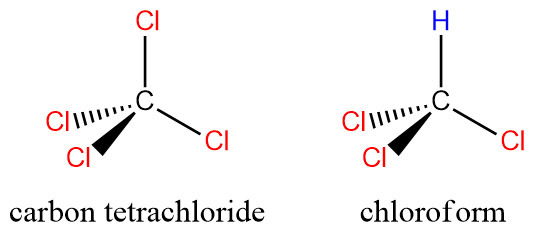
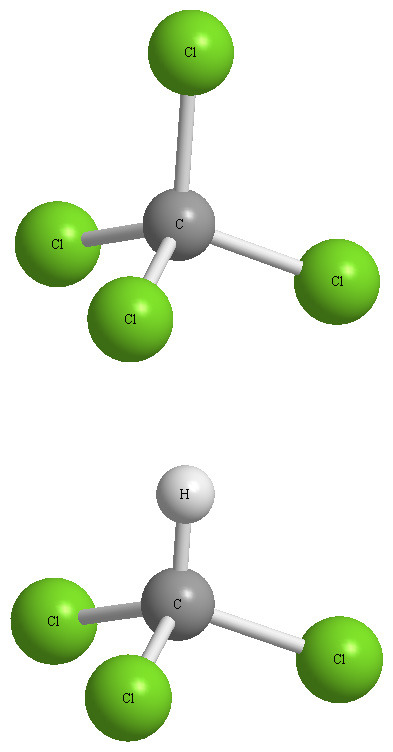
[그림] Molecular geometry of CCl4 and molecular geometry of CHCl3.
CCl4는 무극성 분자, CHCl3는 극성 분자.
( 참고 https://ywpop.tistory.com/7690 )
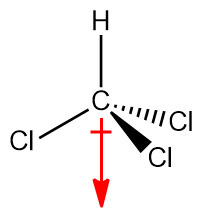
[그림] Dipole moment of CHCl3.
( 참고: CHCl3 루이스 구조 https://ywpop.tistory.com/3745 )
[ 관련 글 https://ywpop.tistory.com/6303 ] CF4 루이스 구조 그리기
[ 관련 글 https://ywpop.tistory.com/11234 ] BH3의 기하구조. 삼각평면
[키워드] CH4 루이스 기준문서, CH4의 구조식, 메탄의 구조식, CH4의 기하구조, 메탄의 기하구조, CH4 기준문서, 메탄 기준문서, 마차 기준문서, 줄다리기 기준문서, CF4 루이스 기준문서, CF4 기준문서, CCl4 루이스 기준문서, CHCl3 루이스 기준문서
'일반화학 > [09장] 분자의 기하구조와 결합 이론' 카테고리의 다른 글
| MO Diagrams of B2, C2, N2 (0) | 2016.05.25 |
|---|---|
| 오존(Ozone, O3)의 루이스 구조 ★ (3) | 2016.05.22 |
| 아질산, HNO2의 루이스 구조 그리기 (0) | 2016.05.16 |
| N2와 N2+의 질소-질소 결합길이 (2) | 2016.04.05 |
| SOCl2 루이스 구조 그리기 (0) | 2015.07.13 |
| CS2 루이스 구조 그리기 (0) | 2015.07.11 |
| 클로로포름(Chloroform, CHCl3)의 루이스 구조 (0) | 2015.07.11 |
| SO3^2- 이온의 루이스 구조 그리기 (6) | 2015.07.08 |




댓글