삼투현상과 삼투압. osmosis and osmotic pressure
---------------------------------------------------
▶ 참고: 제13장 용액의 성질. 목차
[ https://ywpop.tistory.com/15289 ]
---------------------------------------------------
▶ 반투막. semipermeable membrane
> 용매 이동 YES, 용질 이동 NO.
> 예) 세포막
▶ 삼투현상
> 반투막을 통해, 묽은 용액의 용매 분자가 진한 용액 쪽으로 이동하는 현상

[ 그림 출처 commons.wikimedia.org ] Diagram of osmosis in a U-shaped tube through a dialysis membrane when sugar is added to pure water on one side of the membrane.
농도의 개념은 용액 속에 포함된 용질의 양입니다.
즉, 농도가 진하다(높다) 또는 묽다(낮다) 라는 것은
용액 속에 포함된 용질의 양이 상대적으로 많다 또는 적다 입니다.
따라서 고농도라는 것은 용질의 양이 상대적으로 많은 용액이고,
저농도라는 것은 용질의 양이 상대적으로 적은 용액입니다.
저농도 용액의 용매인 물이 반투막을 통해 고농도 용액 쪽으로
이동하는 현상을 삼투현상이라 합니다.
[ 관련 글 https://ywpop.tistory.com/6500 ] 투석
▶ 삼투압(π)
> 삼투현상을 멈추게 하는데 필요한 압력
▶ 삼투압 식은 이상 기체 방정식( PV = nRT )과 비슷...

( 참고: π = MRT https://ywpop.blogspot.com/2024/05/blog-post_21.html )
π = MRT
( 참고 https://ywpop.tistory.com/1921 )
> π = 삼투압(atm), V = 용액의 부피(L), n = 용질의 몰수(mol)
> R = 기체상수(0.08206 atm•L/mol•K), T = 절대온도(K), M = 용액의 몰농도(mol/L)
용질이 전해질인 경우,
π = iMRT
i = 반트호프(van’t Hoff) 인자
( i 설명 https://ywpop.tistory.com/2648 )
[참고] M = WRT / πV

[ 관련 글 https://ywpop.tistory.com/3062 ]
※ 작은 압력이라도 압력은 쉽고, 정확하게 측정할 수 있기 때문에,
삼투압은 물질의 몰질량을 결정할 수 있는 좋은 방법이다.
[ 관련 예제 https://ywpop.tistory.com/6097 ] 베타-카로틴의 몰질량 계산
---------------------------------------------------
[순수한 용매] || [용액] 에서의 삼투압 말고,(||는 반투막)
[용액 A] || [용액 B] 에서의 삼투압인 경우,
> 등장성(isotonic) 용액: 농도가 같은 두 용액
> 고장성(hypertonic) 용액: 농도가 보다 높은 용액
> 저장성(hypotonic) 용액: 농도가 보다 낮은 용액
예) 적혈구를 저장성 용액에 넣으면,
( 따라서 적혈구 내부는 고장성 용액 )
삼투현상에 의해 물이 적혈구 내부로 이동하므로,
적혈구가 팽창 파괴되는 용혈(hemolysis)이 일어나고,
반대로, 적혈구를 고장성 용액에 넣으면,
( 따라서 적혈구 내부는 저장성 용액 )
수축 파괴되는 축혈(crenation)이 일어난다.
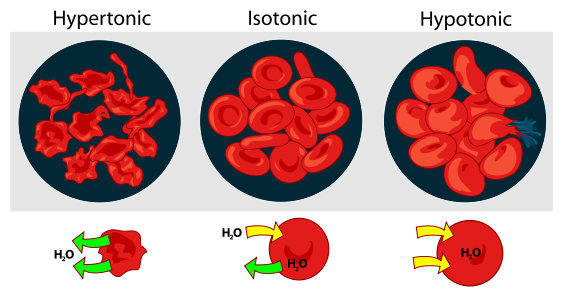
[그림] Osmotic pressure is the hydrostatic pressure produced by a solution in a space divided by a differentially permeable membrane due to a differential in the concentrations of solute.
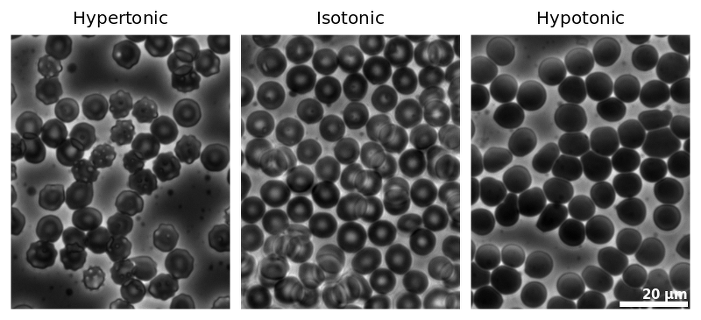
[그림] Human erythrocytes (red blood cells) viewed by phase contrast light microscopy. Three conditions are shown: hypertonic, isotonic and hypotonic conditions.
[ 출처 https://en.wikipedia.org/wiki/Tonicity ]
---------------------------------------------------
[참고] 역삼투압과 역삼투현상
삼투현상을 멈추게 하는데 필요한 압력,
즉 삼투압보다 더 큰 압력으로 누르면 어떻게 될까?
▶ 삼투현상: 반투막을 통해, 묽은 용액의 용매 분자가 진한 용액 쪽으로 이동하는 현상
▶ 삼투압(π): 삼투현상을 멈추게 하는데 필요한 압력
▶ 역삼투압: 삼투압보다 더 큰 압력 (π < 압력)
▶ 역삼투현상: 반투막을 통해, 진한 용액의 용매가 묽은 용액 쪽으로 이동하는 현상
> 삼투압보다 더 큰 압력으로 누르면 (더 큰 압력을 가하면),
진한 용액의 용매가 묽은 용액 쪽으로 이동한다.
> 바닷물의 물이 순수한 물 쪽으로 이동 → 역삼투현상을 이용한 바닷물의 담수화
> 역삼투. Reverse Osmosis (RO)
( 참고: 해수 담수화 https://ywpop.tistory.com/7231 )
[동영상] 삼투 현상과 역삼투 현상.
[ 관련 예제 https://ywpop.tistory.com/search/pi=mrt ] 삼투압 계산
[키워드] 삼투압 기준, pi = mrt 기준, 삼투압 사전, pi = mrt dic, 삼투현상 기준, 삼투현상 사전
'일반화학 > [13장] 용액의 성질' 카테고리의 다른 글
| 벤젠과 톨루엔의 액체 혼합물에서 벤젠 증기의 몰분율 (1) | 2015.06.19 |
|---|---|
| 비휘발성, 비전해질 물질 15 g 물 500 g 0.26℃ (2) | 2015.06.07 |
| 삼투압. 고분자 분자량 측정 (1) | 2015.04.27 |
| 삼투압과 몰질량(분자량). osmotic pressure equation (0) | 2014.12.09 |
| 물에 NaCl 1 mol의 첨가는 글루코스 1 mol보다 증기압력을 더 낮게 한다 (0) | 2014.10.15 |
| 총괄성, 총괄 성질. 반트호프 인자 ★ (4) | 2014.06.30 |
| 증기압 내림과 라울(Raoult)의 법칙 ★ (4) | 2014.06.30 |
| 끓는점오름과 어는점내림 ★ (2) | 2012.09.13 |




댓글