728x170
물질의 상태변화. 승화
[참고] 물질의 상태. States of Matter
[ https://ywpop.tistory.com/15273 ]
일반적인 물질은, 가열하면 (또는 열을 흡수하면),
고체 → 액체 → 기체, 이렇게 상태가 변합니다.
근데, 어떤 물질은, 가열하면 (또는 열을 흡수하면),
고체 → 기체, 이렇게 상태가 변합니다.
즉, 고체에서 액체를 거치지 않고 바로 기체가 됩니다.
이런 현상을 ‘승화’라 하고,
이런 물질을 ‘승화성 물질’이라 합니다.
드라이아이스(고체 CO2), 나프탈렌(좀약)이 대표적인 승화성 물질입니다
( 참고: 상평형도 https://ywpop.tistory.com/2602 )

[ 그림 출처 commons.wikimedia.org ] 상변화. 상태변화.
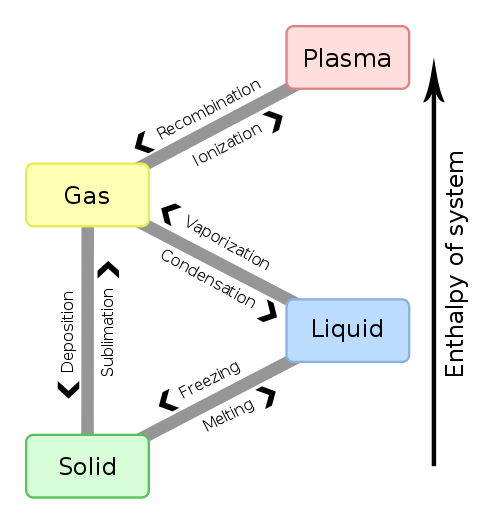
[참고] 승화와 증착. sublimation and deposition
고체 → 액체 상변화를 융해(녹음)라 하고,
이 변화의 반대 과정인
액체 → 고체 상변화를 응고(얼음)라 하듯이,
고체 → 기체 상변화를 ‘승화’라 하고,
이 변화의 반대 과정인
기체 → 고체 상변화를 ‘증착’이라 합니다.
[키워드] 물질의 상태변화 기준문서, 물질의 상태변화 사전, 물질의 상변화 기준문서, 물질의 상변화 사전, 물질의 상전이 기준문서, 물질의 상전이 사전
반응형
그리드형(광고전용)
'일반화학 > [11장] 액체와 분자간의 힘' 카테고리의 다른 글
| 끓는점이 더 높은 것. CO2 또는 CS2 (2) | 2020.05.21 |
|---|---|
| 용융열과 증발열의 합은 승화열과 같다 (0) | 2019.10.25 |
| 분자간 힘과 화학결합을 구별하자 (3) | 2019.05.10 |
| 수소결합 그래프의 2가지 이상한 점. 이걸 어찌 설명할꼬? (0) | 2018.03.14 |
| C2H5OH와 CH3OCH3의 끓는점 비교 (0) | 2017.10.10 |
| 극성분자와 런던분산력 (1) | 2017.09.14 |
| 사이클로펜탄의 끓는점이 n-펜탄보다 더 높은 이유 (0) | 2017.06.06 |
| 분산력과 표면적. 알케인의 끓는점 (1) | 2017.04.17 |



댓글