격자 에너지. Lattice Energy. CaCl2
---------------------------------------------------
▶ 참고: 제8장 화학 결합의 기본 개념. 목차
[ https://ywpop.tistory.com/15249 ]
---------------------------------------------------
▶ 격자 에너지
> 고체 상태의 이온 결합 화합물을
기체 상태의 이온으로 만드는데 필요한 에너지.

▶ 이온 결합 화합물의 안정성 척도
> 격자 에너지 값이 클수록, 안정한 이온 결합 화합물.
▶ 격자 에너지는 쿨롱 힘에 비례하고,
쿨롱 힘은 두 전하의 곱에 비례, 거리에 반비례.
( 참고 https://ywpop.tistory.com/3118 )
▶ 격자 에너지는 직접 측정할 수 없다.
> Hess 법칙에 기초한,
Born-Haber 순환(cycle)을 이용하여 간접적으로 계산.
---> 즉, 이론적(수학적)으로 계산할 수 있다.
▶ 이온 결합 화합물의 격자 에너지 계산 과정
> 이 순서만 기억하면,
격자 에너지 관련 계산 문제는 아무것도 아니다. 너무나 쉽다.
1. 금속 성분의 승화 엔탈피, sublimation enthalpy ... ΔH = + kJ/mol
2. 금속 성분의 이온화 에너지, ionization energy ... ΔH = + kJ/mol
3. 비금속 성분의 결합 해리 엔탈피, bond dissociation enthalpy ... ΔH = + kJ/mol
4. 비금속 성분의 전자 친화도, electron affinity ... ΔH = – kJ/mol
5. 격자 에너지의 역과정, –lattice energy ... ΔH = ? kJ/mol
------------------------------------------------------------------------------
(합) 표준 생성 엔탈피, standard enthalpy of formation ... ΔH = ? kJ/mol

[ 참고: Born–Haber cycle illustrating the enthalpy changes ]
▶ CaCl2의 격자 에너지 계산 과정
1. Ca의 승화 엔탈피, sublimation enthalpy
2.1 Ca의 1차 이온화 에너지, ionization energy
2.2 Ca의 2차 이온화 에너지, ionization energy
3. Cl2의 결합 해리 엔탈피, bond dissociation enthalpy
4. Cl의 전자 친화도, electron affinity
5. 격자 에너지의 역과정, –lattice energy
----------------------------------------------
(합) 표준 생성 엔탈피, standard enthalpy of formation

[주목]
2Cl(g) + 2e^- → 2Cl^-(g) 의 ΔH = 2 × (–364) = –728 kJ/mol
즉, Cl(g)의 전자 친화도 = –364 kJ/mol 의 2배임에 주의할 것.
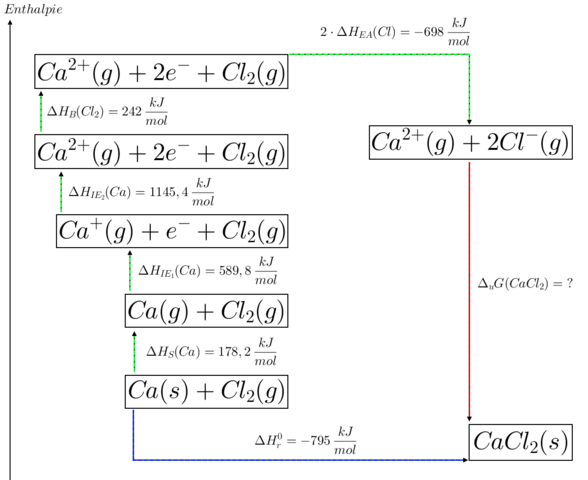
[ 그림 출처 commons.wikimedia.org ] Born-Haber circle process to determine the lattice energy of CaCl2.
[ 관련 글 https://ywpop.tistory.com/7013 ] CaCl의 격자 에너지
[ 관련 예제 https://ywpop.tistory.com/22729 ] CaF2의 격자 에너지
[ 관련 예제 https://ywpop.tistory.com/7225 ] MgF2의 격자 에너지
[ 관련 글 https://ywpop.tistory.com/6061 ] 격자 에너지 도표
[ 관련 예제 https://ywpop.tistory.com/search/격자에너지%20계산%20기준문서 ]
[키워드] CaCl2의 격자 에너지 기준문서, 격자 에너지 계산 기준문서, 일반화학 08장 화학 결합의 기본 개념-1, CaCl2의 격자 에너지 사전, 격자 에너지 계산 사전
'일반화학 > [08장] 화학결합의 기본 개념' 카테고리의 다른 글
| NO3^- 루이스 구조 그리기. 질산 이온 (4) | 2015.07.14 |
|---|---|
| IO3^- 루이스 구조 그리기. iodate ion (0) | 2015.07.13 |
| 확장 팔전자 규칙 또는 18 전자 규칙 ★ (0) | 2015.07.12 |
| 이온 결합 화합물과 분자 화합물 구별 (3) | 2015.04.13 |
| 격자 에너지. Lattice Energy. NaCl ★ (0) | 2015.01.05 |
| 3가지 화학 결합 ★ (1) | 2014.11.29 |
| NH4^+는 극성 분자인가? 쌍극자모멘트 값은? (1) | 2014.11.04 |
| 루이스 전자 점 기호로 나타낸 주기율표 (1) | 2014.10.13 |



댓글