분자간 힘, 반데르발스 힘(van der Waals force) (1)
---------------------------------------------------
▶ 참고: 제11장 액체와 분자간 힘. 목차
[ https://ywpop.tistory.com/15274 ]
---------------------------------------------------

★ 분자간 힘 (intermolecular force)
> 이상 기체: no interaction. But,
> 실제 기체: yes interaction. But, 매우 약하다.
> But, 액체, 고체: 약하지 않다, 상당히 중요하다.
* 응축상 (condensed phases)
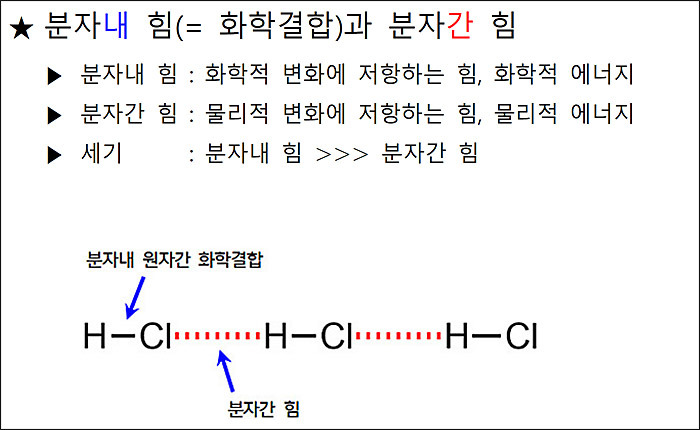
★ 분자내 힘과 분자간 힘
> 분자내 힘(화학 결합) : 화학적 변화에 저항하는 힘, 화학적 에너지
> 분자간 힘: 물리적 변화에 저항하는 힘, 물리적 에너지
> 세기: 분자내 힘 >>> 분자간 힘

★ 그렇다고 무시하지마라, 분자간 힘.
> 물리적 성질을 결정한다.
예) 끓는점, 녹는점, 증기 압력, 점도 등
( 참고: 분자간 힘과 물리적 성질 https://ywpop.tistory.com/23924 )

★ 분자간 힘의 원천
> 쌍극자 (dipole)
> 모든 공유 결합성 분자는 쌍극자를 가질 수 있다.
( 쌍극자의 종류는 다르지만... )
이 때문에
모든 공유결합성 분자 사이에는
쌍극자에 의한 정전기적 인력이 작용한다.

이와 같이,
공유결합성 분자 사이에 작용하는 힘(분자간 힘)을 통칭하여,
“반데르발스 힘”이라고 한다.
반데르발스 힘은 쌍극자의 형태에 따라 3가지로 구분할 수 있다.
① 영구쌍극자-영구쌍극자 힘 [ https://ywpop.tistory.com/2581 ]
② 영구쌍극자-유도쌍극자 힘 [ https://ywpop.tistory.com/2582 ]
③ 순간쌍극자-유도쌍극자 힘 (= London 분산력)
[ https://ywpop.tistory.com/2585 ]
★ 수소 결합 [ https://ywpop.tistory.com/2593 ]
> 영구쌍극자-영구쌍극자 힘의 특수한 형태. 그래서 특별히 강하다.
※ 일반적으로 ‘쌍극자’는 ‘영구쌍극자’를 의미함.
▶ 분자간 힘, 즉 수소 결합을 포함한 모든 반데르발스 힘은
분자내 원자간 결합(= 화학 결합)인 공유 결합에 비하면,
( 참고: 화학 결합 https://ywpop.tistory.com/5995 )
새 발의 피만큼도 못한 아주 약한 힘이다.
( 각 힘의 평균값으로 비교했을 경우 )
[ 관련 글 https://ywpop.tistory.com/12291 ] 이온-쌍극자 힘. ion-dipole force
[ 관련 글 https://ywpop.tistory.com/5954 ] 분자간 힘 크기 순서. 분자간 힘 세기 순서
[ 관련 글 https://ywpop.tistory.com/11284 ] 분자간 힘과 화학결합을 구별하자
[키워드] 분자간 힘 기준문서, 분자간힘 기준문서, 분자간 힘 사전, 분자간힘 사전
'일반화학 > [11장] 액체와 분자간의 힘' 카테고리의 다른 글
| 물의 상평형도 (phase diagram of water) (0) | 2014.06.14 |
|---|---|
| 상평형도(phase diagram) (0) | 2014.06.13 |
| 임계 온도와 임계 압력 (4) | 2014.06.13 |
| 물의 높은 끓는점과 수소 결합 (0) | 2014.06.12 |
| 수소 결합 (hydrogen bond) ★ (0) | 2014.06.09 |
| 분자의 크기와 분산력, 끓는점 비교 (0) | 2014.06.05 |
| 순간 쌍극자와 London 분산력 ★ (0) | 2014.06.04 |
| 유도쌍극자, 유발쌍극자, 분극성, 편극성 (0) | 2014.06.03 |




댓글