redox balance. Cu(NH3)4^2+ + S2O4^2- → SO3^2- + Cu + NH3 (basic)
산화-환원 반응 완성하기. S2O4^2- + Cu(NH3)4^2+ → SO3^2- + Cu + NH3
Balance the following redox in a basic solution
Cu(NH3)4^2+ + S2O4^2- → SO3^2- + Cu + NH3
---------------------------------------------------
▶ 참고: 산화-환원 반응 균형 맞추기 (염기성 용액)
[ https://ywpop.tistory.com/6321 ]
---------------------------------------------------
1. 반쪽 반응식 나누기
산화: S2O4^2- → SO3^2- (S의 산화수는 +3에서 +4로 증가, S2O4^2-는 산화됨.)
환원: Cu(NH3)4^2+ → Cu (Cu의 산화수는 +2에서 0으로 감소, Cu(NH3)4^2+는 환원됨.)
( 참고: S의 산화수 https://ywpop.tistory.com/9966 )
2. 질량 균형 맞추기
산화: S2O4^2- + 2H2O → 2SO3^2- + 4H^+
환원: Cu(NH3)4^2+ → Cu + 4NH3
3. 전하 균형 맞추기
산화: S2O4^2- + 2H2O → 2SO3^2- + 4H^+ + 2e^-
환원: Cu(NH3)4^2+ + 2e^- → Cu + 4NH3
4. 주고받은(이동한) 전자 수 같도록. 이미 같음.
산화: S2O4^2- + 2H2O → 2SO3^2- + 4H^+ + 2e^-
환원: Cu(NH3)4^2+ + 2e^- → Cu + 4NH3
5. 반쪽 반응 더하기
Cu(NH3)4^2+ + S2O4^2- + 2H2O → 2SO3^2- + Cu + 4NH3 + 4H^+
6. H^+를 OH^-로 바꾸기 (∵ 염기성 용액). 끝.
Cu(NH3)4^2+ + S2O4^2- + 2H2O + 4OH^- → 2SO3^2- + Cu + 4NH3 + 4H^+ + 4OH^-
Cu(NH3)4^2+ + S2O4^2- + 2H2O + 4OH^- → 2SO3^2- + Cu + 4NH3 + 4H2O
Cu(NH3)4^2+ + S2O4^2- + 4OH^- → 2SO3^2- + Cu + 4NH3 + 2H2O
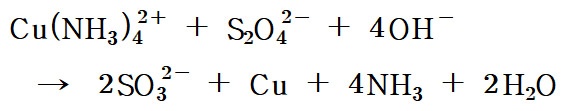
[키워드] redox Cu(NH3)4^2+ + S2O4^2-, redox S2O4^2- + Cu(NH3)4^2+
'일반화학 > [20장] 전기화학' 카테고리의 다른 글
| redox balance. Br2 → BrO3^- + Br^- (basic) (0) | 2018.12.16 |
|---|---|
| redox balance. CN^- + MnO4^- → CNO^- + MnO2 (basic) (0) | 2018.12.15 |
| 기전력과 자유에너지 사이의 관계 ★ (0) | 2018.11.05 |
| redox balance. ClO3^- → Cl2 + O2 (acidic) (1) | 2018.11.01 |
| redox balance. Mg + CO2 → MgO + C (dry ice) (0) | 2018.10.03 |
| redox balance. CuO + C → Cu + CO2 (acidic) (0) | 2018.10.03 |
| redox balance. N2H4 + N2O4 → N2 + H2O (0) | 2018.09.25 |
| redox balance. C8H18 + O2 → CO2 + H2O (0) | 2018.09.25 |




댓글