HNO3의 루이스 구조와 형식전하. HNO3의 산화수
HNO3 Lewis structure (nitric acid)
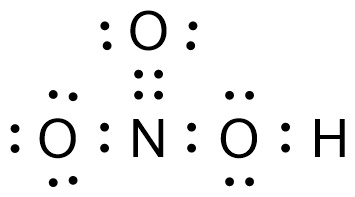

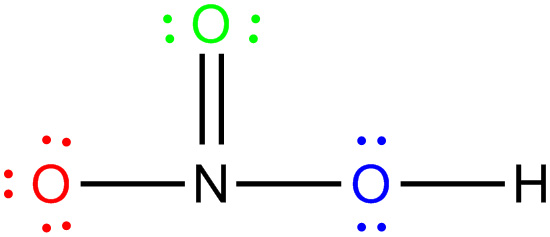
[그림] HNO3의 루이스 구조.
A. HNO3의 형식전하
형식전하 = 원자가전자수 – 비결합전자수 – (결합전자수/2)
( 참고 https://ywpop.tistory.com/2544 )
> N의 형식전하 = 5 – 0 – 4 = +1
> O(red)의 형식전하 = 6 – 6 – 1 = –1
> O(green)의 형식전하 = 6 – 4 – 2 = 0
> O(blue)의 형식전하 = 6 – 4 – 2 = 0
> H의 형식전하 = 1 – 0 – 1 = 0
B. HNO3의 산화수
( 참고: 산화수 구하는 규칙 https://ywpop.tistory.com/2719 )
HNO3 에서,
H의 산화수 = +1 (넘버 2) 이고,
O의 산화수 = –2 (넘버 3) 이므로,
(H) + (N) + 3(O) = 0
(+1) + (N) + 3(–2) = 0
따라서
N의 산화수 = +5.
[참고] 전기음성도로 산화수를 계산하면 오류 발생
전기음성도 차이로 질소의 산화수를 계산하면, +4가 나온다.
[참고] HNO3의 공명 구조

공명 구조는 형식 전하가 존재한다는 불안정성을 극복하게 해준다.
즉, 공명 구조 존재로 인한 안정성 >>> 형식 전하 존재로 인한 불안정성
[ 관련 글 https://ywpop.blogspot.com/2024/05/peroxynitrous-acid-hno3.html ]
Peroxynitrous acid (HNO3)의 루이스 구조

[ 관련 글 https://ywpop.blogspot.com/2024/06/drawing-lewis-structure-of-hno3-nitric.html ]
HNO3 루이스 구조 그리기

[키워드] HNO3 루이스 기준, HNO3 루이스 구조 기준, 질산 루이스 기준, 질산 루이스 구조 기준
'일반화학 > [08장] 화학결합의 기본 개념' 카테고리의 다른 글
| FeBr3는 이온결합 화합물 ★ (0) | 2018.04.21 |
|---|---|
| 팔전자 규칙의 예외. 옥텟 규칙의 예외 ★ (0) | 2018.02.12 |
| 이온 결합 화합물의 녹는점 비교 ★ (0) | 2017.12.15 |
| 격자에너지. KCl MgO. MgO KCl (0) | 2017.11.30 |
| 배위 공유 결합. NH4^+와 H3O^+ (1) | 2017.10.05 |
| 단일결합과 다중결합의 결합세기(결합힘, 결합에너지) (0) | 2017.10.04 |
| 베릴륨 화합물. BeF2, BeCl2는 공유결합 물질 ★ (0) | 2017.10.01 |
| N2O 루이스 구조 그리기 (1) | 2017.06.16 |



댓글