팔전자 규칙의 예외. 옥텟 규칙의 예외
1. 원자가전자가 8개 보다 작은 분자와 이온
A. 홀수 개의 전자를 가진 분자와 이온 (odd number of electrons)
예: NO, NO2
( NO 설명 https://ywpop.tistory.com/10503 )
( NO2 설명 https://ywpop.tistory.com/10314 )
B. 원자가전자가 8개 보다 작은 분자와 이온 (less than an octet of electrons)
▶ H, Be, B (각각 2, 4, 6개 공유 결합 전자)
예: H2, BeH2, BF3

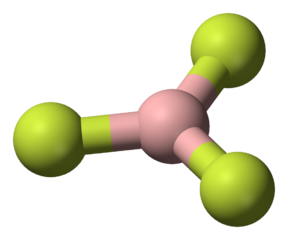
[ 그림 출처: commons.wikimedia.org ] BF3는 무극성 분자.
[ 관련 글 https://ywpop.tistory.com/11234 ] BH3의 기하구조
> Be는 원자가전자 수가 2개뿐이기 때문에,
sp 혼성을 통해 주변에 최대 4개의 전자를 가질 수 있다.
> B는 원자가전자 수가 3개뿐이기 때문에,
sp^2 혼성을 통해 주변에 최대 6개의 전자를 가질 수 있다.
> Be와 B는 2주기 원소이므로,
S와 같은 3주기 원소처럼 비어있는 d 오비탈이 없기 때문에,
설령 주위 원자가 비공유 전자쌍을 갖고 있더라도,
그 비공유 전자쌍을 당겨와서 사용할 수 없다.
( 참고: SO3 루이스 구조 https://ywpop.tistory.com/3820 )
[참고] duet rule. 듀엣 규칙
Because hydrogen only needs two electrons to fill its valence shell, it follows the “duet rule”. It is an exception to the octet rule. Hydrogen only needs to form one bond. This is the reason why H is always a terminal atom and never a central atom.

[그림 NH3 루이스 전자 점 구조.
> N은 옥텟 규칙 만족.
> H는 듀엣 규칙 만족(옥텟 규칙 예외).
2. 원자가전자가 8개 보다 많은 분자와 이온
▶ 팔전자보다 많은 전자 (more than an octet of electrons)
- 확장 팔전자 규칙 또는 18 전자 규칙
( 관련 글 https://ywpop.tistory.com/3752 )
▶ s, p 뿐만 아니라 d 오비탈까지 결합에 이용.
8 + 10(d 오비탈) = 18 전자
▶ 한 원자가 최대 18 전자까지 가질 수 있다.
(18 전자를 다 가져야만 하는 것은 아님에 주의)
예: PF5, SF6
[ 관련 글 https://ywpop.tistory.com/41 ] 옥텟 규칙의 예외 (P, S, Cl)
[ 관련 글 https://ywpop.tistory.com/5627 ] 전이원소의 옥텟규칙
옥텟 규칙 예외. 모든 원자가 옥텟 규칙을 따르지는 않는다. 소수의 일부 원자만 옥텟 규칙을 따른다.
[키워드] 옥텟 룰의 예외 기준문서, 옥텟 규칙의 예외 기준문서, 옥텟 규칙 기준문서, 팔전자 규칙 예외 기준문서, 옥텟 규칙 예외 기준문서, 옥텟 규칙 예외 사전, 팔전자 규칙 예외 사전, 옥텟 예외 기준문서, 팔전자 예외 기준문서, 옥텟 예외 사전, 팔전자 예외 사전, BF3 기준문서, BF3 dic
'일반화학 > [08장] 화학결합의 기본 개념' 카테고리의 다른 글
| 브로민 원자간의 화학 결합을 깨는데 필요한 빛의 파장 (0) | 2018.05.24 |
|---|---|
| CsF의 격자에너지. 생성엔탈피 계산 (2) | 2018.05.18 |
| 격자에너지. LiCl KCl KBr MgCl2 (2) | 2018.05.16 |
| FeBr3는 이온결합 화합물 ★ (0) | 2018.04.21 |
| 이온 결합 화합물의 녹는점 비교 ★ (0) | 2017.12.15 |
| 격자에너지. KCl MgO. MgO KCl (0) | 2017.11.30 |
| HNO3의 루이스 구조와 형식전하. HNO3의 산화수 (0) | 2017.10.07 |
| 배위 공유 결합. NH4^+와 H3O^+ (1) | 2017.10.05 |


댓글