결합엔탈피로 반응엔탈피 계산. C2H4 + H2 → C2H6
bond enthalpy and enthalpy of reaction
다음 반응에 대하여 다음 문제를 푸시오.
H2(g) + C2H4(g) → C2H6(g)
a) 결합 에너지 값을 이용하여 반응 엔탈피를 계산하시오.
b) 표준 생성 엔탈피를 이용하여 반응 엔탈피를 계산하시오.
(C2H4, C2H6의 ΔH°_f는 각각 52.3 kJ/mol, –84.7 kJ/mol이다.)
c) a)와 b)의 반응 엔탈피 값이 차이나는 이유를 설명하시오.
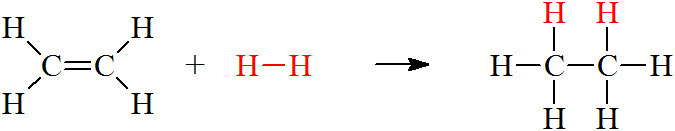
a)
ΔH_rxn = Σ(절단 결합의 결합 엔탈피) – Σ(생성 결합의 결합 엔탈피)
= [ (C=C) + 4(C–H) + (H–H) ] – [ (C–C) + 6(C–H) ]
= [ (611) + 4(410) + (436) ] – [ (350) + 6(410) ]
= [ 2687 ] – [ 2810 ]
= –123 kJ
( 참고 https://ywpop.tistory.com/3729 )
또는
= [ (C=C) + 4(C–H) + (H–H) ] – [ (C–C) + 6(C–H) ]
= [ (620) + 4(414) + (436.4) ] – [ (347) + 6(414) ]
= –118.6
= –119 kJ
b)
ΔH°_rxn = [생성물들의 ΔH°_f 합] – [반응물들의 ΔH°_f 합]
= [ΔH°_f(C2H6,g)] – [ΔH°_f(C2H4,g)]
= [–84.7] – [52.3]
= –137.0 kJ
( 참고 https://ywpop.tistory.com/3431 )
c)
a) 계산에 사용된 결합 엔탈피는 실제값(exact value)이 아닌 평균값이기 때문이다.
이 때문에 평균결합 엔탈피 값으로 계산한 반응 엔탈피 값과
표준생성 엔탈피 값으로 계산한 반응 엔탈피 값은 약간 차이가 발생한다.
( 참고 https://ywpop.tistory.com/2559 )
[참고]
생성 엔탈피는 어떤 화합물이 그것을 이루는 원소로부터 생성될 때(결합 생성)의 엔탈피 변화이고,
( 참고 https://ywpop.tistory.com/4416 )
결합 에너지는 화합물 내 특정 결합을 파괴시키는데 필요한 에너지입니다.
( 참고 https://ywpop.tistory.com/2558 )
즉, 생성 엔탈피는 “결합 생성”, 결합 에너지는 “결합 파괴”로,
서로 반대 과정이므로,
한 방법이 “생성물의 값 – 반응물의 값”으로 계산하면,
다른 방법은 “반응물의 값 – 생성물의 값”으로 계산해야지,
둘 다 동일한 부호를 갖는 ΔH의 결과가 나옵니다.
[ 관련 글 https://ywpop.tistory.com/13107 ] 반응 엔탈피를 계산하는 2가지 방법
[키워드] 평균결합에너지 기준, 평균결합엔탈피 기준, 결합엔탈피로 반응엔탈피 기준, 생성엔탈피로 반응엔탈피 기준, 반응 엔탈피 계산 기준, 2가지 반응 엔탈피 기준, 반응물 – 생성물 기준, 생성물 – 반응물 기준, ΔH 계산. H2 + C2H4 → C2H6, ΔH 계산. H2(g) + C2H4(g) → C2H6(g), ΔH 계산. C2H4 + H2 → C2H6, ΔH 계산. C2H4(g) + H2(g) → C2H6(g)
'일반화학 > [05장] 열화학' 카테고리의 다른 글
| 열용량과 비열. 얼음, 물, 수증기의 비열 자료, 잠열 자료 (0) | 2018.09.14 |
|---|---|
| 열용량과 비열. 18.61 kg 철 100℃ 가열 (2) | 2018.09.09 |
| 결합엔탈피로 반응엔탈피 계산. 에탄올의 연소엔탈피 (0) | 2018.08.14 |
| 상태함수와 경로함수 (0) | 2018.06.19 |
| 생성엔탈피로 반응엔탈피 계산. C3H8(g) + O2(g) (1) | 2018.05.30 |
| 결합엔탈피로 반응엔탈피 계산. 2CO + O2 → 2CO2 (0) | 2018.05.22 |
| 금속의 비열. 1012 g의 금속 조각에 69.5 kJ (0) | 2018.05.09 |
| 열용량과 비열. 마그네슘 금속 0.243 g을 충분한 양의 HCl과 혼합 (0) | 2018.04.19 |


댓글