르 샤틀리에(Le Chatelier)의 원리. 온도 변화
발열(exothermic) vs. 흡열(endothermic) 반응에서...
C. 온도의 변화
▶ 농도, 부피/압력의 변화는 평형의 위치는 변화시키되
평형 상수 값에는 영향을 미치지 않는다.
그러나 온도의 변화는 평형 상수 값을 변하게 한다.
▶ 온도를 변화시키면,
[1] 반응은 어느 방향으로 진행할까?
[2] 이때 평형 상수, K 값은 증가할까? 감소할까?
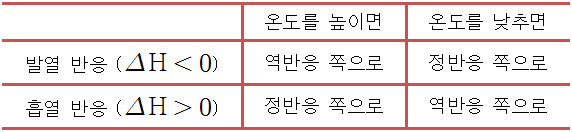
▶ 먼저, 온도를 변화시켰을 때 반응 진행 방향을 정리하면,
① 발열 반응일 때, 온도를 증가시키면: 역반응 쪽으로 반응 진행
② 흡열 반응일 때, 온도를 증가시키면: 정반응 쪽으로 반응 진행
▶ 르 샤틀리에의 원리를 적용하기 위한 간단한 방법
---> 열을 반응물 또는 생성물 중 하나인 물질로 취급.
( 발열 반응 → 열이 발생한다. → (생성물처럼) 열이 만들어진다. )
▶ 열화학 반응식에서 반응열, Q는 다음과 같이 나타낸다.
① 발열 반응: 반응물 ⇌ 생성물 + Q
② 흡열 반응: 반응물 + Q ⇌ 생성물
( 참고: 열화학 반응식 https://ywpop.tistory.com/6398 )
① 발열 반응: 반응물 ⇌ 생성물 + Q
> Q는 생성물 쪽에 있다.
> 열 ≡ 생성물
> 가열 또는 온도 증가 ≡ 생성물 추가 또는 증가
---> 역반응이 일어난다.
② 흡열 반응: 반응물 + Q ⇌ 생성물
> Q는 반응물 쪽에 있다.
> 열 ≡ 반응물
> 가열 또는 온도 증가 ≡ 반응물 추가 또는 증가
---> 정반응이 일어난다.
▶ 평형 상태에서, 계의 온도(Q)를 증가시킨다는 것은...
① 발열 반응: 생성물 추가(증가) ⇨ 역반응이 일어난다.
② 흡열 반응: 반응물 추가(증가) ⇨ 정반응이 일어난다.
▶ 다음으로, 온도를 변화시켰을 때
평형 상수 값이 어떻게 변하는 지 다음 예를 통해 살펴보자.

▶ 온도를 변화시켰을 때 평형 상수 값 변화를 정리하면,
① 발열 반응일 때, 온도를 증가시키면: 평형 상수, K 감소.
② 흡열 반응일 때, 온도를 증가시키면: 평형 상수, K 증가.
[ 관련 예제 https://ywpop.tistory.com/10718 ]
[ A. 농도 변화 https://ywpop.tistory.com/2685 ]
[ B. 부피/압력 변화(1) https://ywpop.tistory.com/2686 ] PV = k
[ B. 부피/압력 변화(2) https://ywpop.tistory.com/2690 ] 강철 용기. 비활성 기체
[ C. 온도 변화 https://ywpop.tistory.com/2691 ]
[ 르샤틀리에의 원리 종합 예제 https://ywpop.tistory.com/12328 ]
[키워드] 르 샤틀리에 기준문서, 르 샤틀리에 원리 기준문서, 르 샤틀리에의 원리 기준문서, 온도 변화 효과 기준문서, 온도 효과 기준문서
'일반화학 > [15장] 화학 평형' 카테고리의 다른 글
| 800 K I2(g) ⇌ 2I(g) Kc = 3.1×10^(-5) 10.0 L 2.67×10^(-2) g I(g) (2) | 2015.10.07 |
|---|---|
| 순수한 액체와 고체의 농도가 평형 상수 표현에 포함되지 않는 이유 ★ (0) | 2015.07.14 |
| 평형상수. 아세트산에틸(ethyl ethanoate)의 제조 (3) | 2015.05.17 |
| 평형에서의 농도. 일산화탄소와 수소 혼합물(합성가스) (0) | 2015.05.14 |
| 르 샤틀리에(Le Chatelier)의 원리. 부피/압력 변화 (4) | 2014.07.17 |
| 르 샤틀리에(Le Chatelier)의 원리. 부피/압력 변화 (3) | 2014.07.16 |
| 르 샤틀리에(Le Chatelier)의 원리. 농도 변화 ★ (1) | 2014.07.15 |
| 화학 평형과 물리 평형 (0) | 2014.07.14 |




댓글