VSEPR. 메탄올의 결합각
---------------------------------------------------
▶ 참고: VSEPR. 큰 분자의 기하구조 예측
[ https://ywpop.tistory.com/7670 ]
---------------------------------------------------
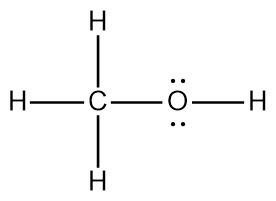
[그림] 메탄올의 루이스 구조.
C와 O의 전자영역(입체수) = 4 이므로,
( C와 O의 혼성오비탈 = sp^3 )
( 참고 https://ywpop.tistory.com/11542 )
메탄올의 모든 결합각 = ~109.5°
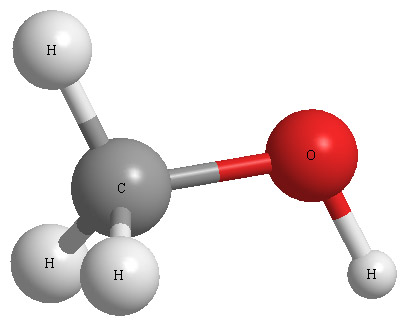
[그림] 3D model of CH3OH molecule structure.
▶ C의 전자영역 = 4
> 이론 ∠H–C–H = ~109.5°
> 이론 ∠H–C–O = ~109.5°
▶ O의 전자영역 = 4
> 이론 ∠C–O–H = ~109.5°
> O에 존재하는 2개 비공유전자쌍의 더 큰 반발력 때문에,
( 참고 https://ywpop.tistory.com/2571 )
실제 ∠C–O–H < 109.5°
▶ Experimental values for the bond angles
> 109.03°±0.75° for the angle formed by H–C–H
> 108.87°±2° for the angle formed by H–O–C
( 출처 https://cms.gutow.uwosh.edu/gutow/P-Chem_Web_Posters/KSSG/methanol%20script/methanol%20script.html )
[키워드] 메탄올의 결합각 기준, 메탄올의 결합각도 기준, 메탄올 루이스 기준, 거대 분자 기준
'일반화학 > [09장] 분자의 기하구조와 결합 이론' 카테고리의 다른 글
| BF4^- 루이스 구조 그리기 (0) | 2022.09.26 |
|---|---|
| PHCl2 루이스 구조 그리기 (0) | 2022.09.24 |
| ClO2^- 루이스 구조 그리기 (0) | 2022.09.15 |
| 분자의 화학식으로부터 분자의 기하구조 예측 (1) | 2022.09.07 |
| N3^- NO2^- I3^- 루이스 구조 (0) | 2022.08.10 |
| AlCl3의 공명 구조 (0) | 2022.06.16 |
| N2와 O2의 MO. σ_2p MO와 π_2p MO의 위치 (1) | 2022.06.16 |
| PF3 루이스 구조 (0) | 2022.06.15 |


댓글