5 mM 포름산 용액 1 L 만들기
0.005 M 폼산 용액 1 L 만들기
---------------------------------------------------
(0.005 mol/L) (1 L) = 0.005 mol 포름산
( 참고 https://ywpop.tistory.com/7787 )
포름산, HCOOH의 몰질량 = 46.03 g/mol 이고,
포름산의 밀도 = 1.22 g/mL 이므로,
(0.005 mol) × (46.03 g/mol) / (1.22 g/mL)
= (0.005) × (46.03) / (1.22)
= 0.19 mL
---> 0.005 M 폼산 용액 1 L 제조에 필요한 시약의 부피
[용액 제조에 필요한 시약의 부피 계산 공식]
시약의 순도 = 95% 라 가정하면,
시약의 부피(mL) = 몰농도 × 부피(L) × 몰질량 / (순도%/100) / 밀도
= 0.005 × 1 × 46.03 / (95/100) / 1.22
= 0.20 mL
[용액 제조 방법]
1) 제조하려는 용액의 부피에 해당하는 부피 플라스크에다가
제조하려는 용액의 부피의 대략 1/2에 해당하는 증류수를 가한다.
2) 위에서 계산한 시약의 부피를 천천히 가한다.
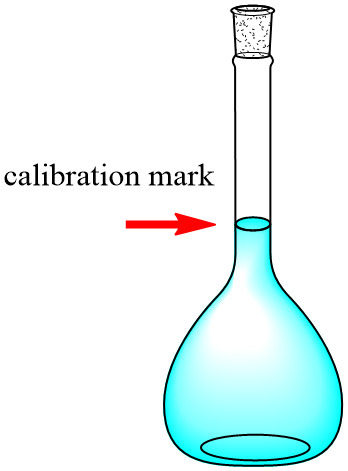
3) 부피 플라스크의 표선(calibration mark)까지 증류수를 마저 채운다. 끝.
( 참고 https://ywpop.tistory.com/6158 )
[참고] HCOOH의 당량수 = 1 eq/mol 이므로,
HCOOH의 몰농도 = HCOOH의 노르말농도.
( 참고: 당량수 https://ywpop.tistory.com/4105 )
따라서 0.005 M 포름산 용액 1 L 제조방법과
0.005 N 포름산 용액 1 L 제조방법은 100% 동일하다.
[키워드] 포름산 기준문서, 포름산 몰농도 기준문서, 포름산 노르말농도 기준문서, 포름산 사전, 포름산 몰농도 사전, 포름산 노르말농도 사전, 폼산 기준문서, 폼산 몰농도 기준문서, 폼산 노르말농도 기준문서, 폼산 사전, 폼산 몰농도 사전, 폼산 노르말농도 사전
'화학 > 용액의 농도' 카테고리의 다른 글
| 물 500 mL에 NaCl 3 g 녹아있는 용액의 ppm 농도 (0) | 2022.08.01 |
|---|---|
| 160 mM KCl 용액 100 mL 만들기 (0) | 2022.07.26 |
| 444 ppm SO2 유량 52 m3/h 하루 배출 SO2 (kg) (1) | 2022.07.25 |
| 1% w/w NaCl 농도를 mg/L 농도로 환산 (0) | 2022.07.22 |
| 황산 시료 1 g을 증류수로 묽혀서 NaOH 용액으로 적정 (0) | 2022.07.20 |
| 2.0 M NH3 (3 mL), 탈이온수(12 mL)를 혼합한 용액의 pH (0) | 2022.07.18 |
| H2SO4 시료의 순도 결정 (0) | 2022.07.17 |
| 중화적정에 사용할 표준 산으로 0.1 N 옥살산을 만들려고 한다 (0) | 2022.07.15 |
댓글