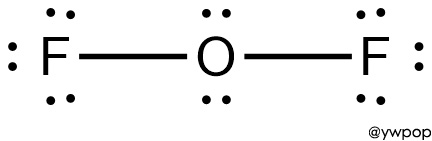
OF2의 루이스 구조식
Lewis structure of OF2, oxygen difluoride

[그림] OF2의 루이스 구조식.
( 참고: 옥텟 규칙 https://ywpop.tistory.com/2634 )

[그림] Lewis dot structure of OF2.
[참고] 루이스 전자 점 기호로 나타낸 주기율표
[ https://ywpop.tistory.com/2872 ]
---------------------------------------------------
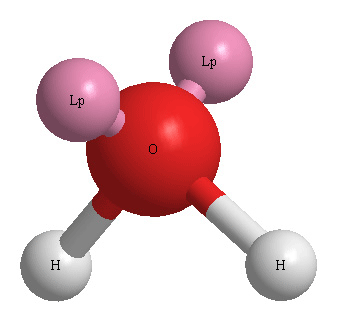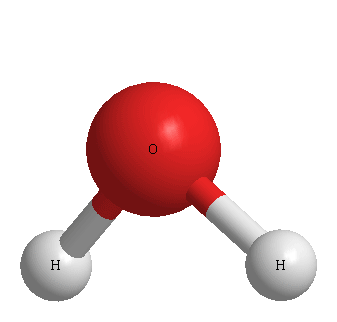
[그림] H2O의 기하구조.
OF2의 루이스 구조와
H2O의 루이스 구조는
( 그림 https://ywpop.tistory.com/2569 )
100% 같으므로,
두 분자의 기하구조도 같다.
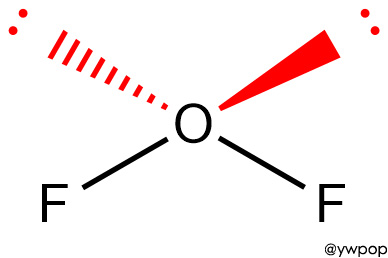
▶ 분자의 기하구조는 둘 다 ‘굽은형’이며,
비공유 전자쌍(Lp = lone pair)을 포함한
전자 영역의 기하구조는 둘 다 ‘사면체’이다.
▶ 중심 원자 O의 공유 전자쌍 = 2개, 비공유 전자쌍 = 2개
---> 전자 영역의 기하구조는 사면체.
---> 분자의 기하구조는 굽은형.
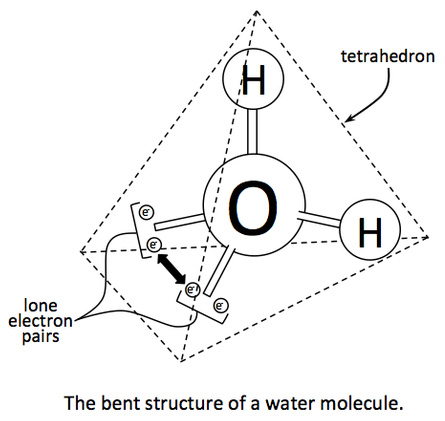
▶ 중심 원자의 혼성화
> 중심 원자 O의 전자영역 = 4
---> sp3 혼성오비탈
( 참고 https://ywpop.tistory.com/11542 )
▶ 분자의 기하구조
> sp3 혼성오비탈
---> 전자 영역의 기하구조 = 정사면체.
> 비공유 전자쌍이 2개이므로,
---> 분자의 기하구조 = 굽은형.
---------------------------------------------------

[그림] H2O와 OF2의 쌍극자 모멘트 방향.
분자의 극성은 결합의 쌍극자 모멘트의 ‘벡터 합’으로 결정.
벡터 합 = 0 이면, 무극성,
벡터 합 > 0 이면, 극성.
H2O와 OF2는 “벡터 합 > 0” 이므로, 극성 분자.
[참고] 쌍극자 모멘트, dipole moment
> dipole moment of H2O = 2.39 D
> dipole moment of OF2 = 0.31 D
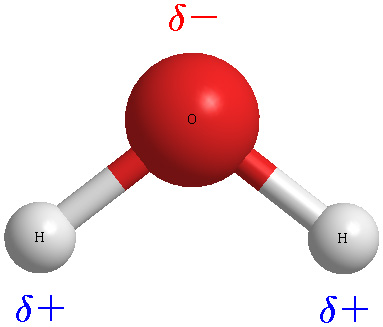
[그림] dipole moment of the water (H2O).
[참고] OF2 electrolyte or nonelectrolyte
oxygen difluoride electrolyte or nonelectrolyte
OF2 자체는 공유결합 화합물이므로,
물에서 이온화 되지 않기 때문에,
OF2는 전기 전도성이 없다.
그러나, 매우 느리지만, 가수분해를 고려하면,
Oxygen difluoride reacts very slowly with water
to form hydrofluoric acid:
OF2 + H2O → 2HF + O2
---> 생성된 HF 때문에, OF2 수용액은 전기 전도성이 있다.
[ 관련 글 https://ywpop.blogspot.com/2024/06/co2-non-polar-molecule-of2-polar.html ]
OF2의 루이스 구조. OF2의 기하 구조
[키워드] OF2 루이스 구조 기준, H2O 루이스 구조 기준, OF2 루이스 기준, H2O 루이스 기준
'일반화학 > [09장] 분자의 기하구조와 결합 이론' 카테고리의 다른 글
| FNO의 루이스 구조. Lewis structure of FNO ★ (0) | 2018.07.12 |
|---|---|
| 삼염화질소의 루이스 구조. nitrogen trichloride. NCl3 (0) | 2018.07.10 |
| BeH2의 혼성 오비탈. 베릴륨의 혼성화. Be의 sp 혼성 오비탈 (1) | 2018.07.06 |
| 원자 오비탈(AO)의 혼성화 이론 정리 (3) | 2018.06.08 |
| Lewis structure of HClO4, HClO3, HClO2, and HClO (0) | 2018.02.13 |
| VSEPR. 큰 분자의 기하구조 예측 (0) | 2017.10.07 |
| SF6 혼성 오비탈 (hybrid orbitals) (1) | 2017.07.22 |
| SF4 혼성 오비탈 (hybrid orbitals) (2) | 2017.07.22 |



댓글