NO3^- 루이스 구조 그리기(2). O–N–O–O 직선형
Lewis structure of NO3^-. nitrate ion
---------------------------------------------------
▶ 참고: 루이스 구조 그리기
[ https://ywpop.tistory.com/6302 ]
---------------------------------------------------
▶ 참고: NO3^- 루이스 구조 그리기. 삼각 평면형
[ https://ywpop.tistory.com/3766 ]
[1단계] 각 원자의 원자가전자 수의 합을 구한다.
① 양이온이면, 전하 수만큼 빼고,
② 음이온이면, 전하 수만큼 더한다.
NO3^- = 5 + 3(6) + 1 = 24
[2단계] 화합물의 기본 골격 구조를 그린다.
( 단일결합 수만큼 전자 수를 뺀다. )

24 – 3(2) = 18
[3단계] 주위 원자들이 팔전자 규칙에 맞도록 전자를 한 쌍씩 그린다.
( 무조건, 그냥 주위 원자 주변에 전자쌍 3개씩 그린다. )
( 그린 전자 수만큼 뺀다. )

18 – 6 – 4 – 6 = 2
[4단계] 중심 원자도 팔전자 규칙에 맞도록 그린다.
중심 원자도 팔전자 규칙에 맞나? Yes → Stop.
중심 원자도 팔전자 규칙에 맞나? No → 3단계에서 남은 원자가전자가 있나?
① Yes → 중심 원자에 전자 한 쌍씩 그린다, 모두 사용할 때까지.
② No → 주위 원자의 비결합전자쌍을 사용하여 이중 또는 삼중 결합을 그린다,
중심 원자도 팔전자 규칙에 맞을 때까지.

중심 원자 N에 남아있는 2개 전자를 그려넣어도
팔전자 규칙에 맞지 않다, 부족하다.
주위 원자의 비결합전자쌍을 사용하는 3가지 구조를 그려보면...
[참고] 형식 전하 계산
형식전하 = 원자가전자수 – 비결합전자수 – (결합전자수/2)
( 참고 https://ywpop.tistory.com/2544 )

▶ 1번 직선형 구조
( 산소 원자는 좌에서 우로, 1, 2, 3, 숫자를 붙여서 구분. )
> N의 형식전하 = 5 – 2 – (6/2) = 0
> O(1)의 형식전하 = 6 – 4 – (4/2) = 0
> O(2)의 형식전하 = 6 – 4 – (4/2) = 0
> O(3)의 형식전하 = 6 – 6 – (2/2) = –1
---> 가장 안정한 직선형 구조
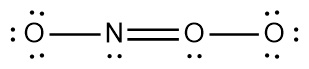
▶ 2번 직선형 구조
> N의 형식전하 = 5 – 2 – (6/2) = 0
> O(1)의 형식전하 = 6 – 6 – (2/2) = –1
> O(2)의 형식전하 = 6 – 2 – (6/2) = +1
> O(3)의 형식전하 = 6 – 6 – (2/2) = –1
---> 형식전하를 가진 원자가 더 많기 때문에,
불안정한 구조.
---> O(2)의 결합 수가 3이기 때문에,
처음부터 불가능한 구조.
( O의 최대 결합 수는 2 )
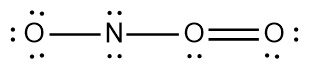
▶ 3번 직선형 구조
> N의 형식전하 = 5 – 4 – (4/2) = –1
> O(1)의 형식전하 = 6 – 6 – (2/2) = –1
> O(2)의 형식전하 = 6 – 2 – (6/2) = +1
> O(3)의 형식전하 = 6 – 4 – (4/2) = 0
---> 형식전하를 가진 원자가 더 많기 때문에,
불안정한 구조.
---> O(2)의 결합 수가 3이기 때문에,
처음부터 불가능한 구조.
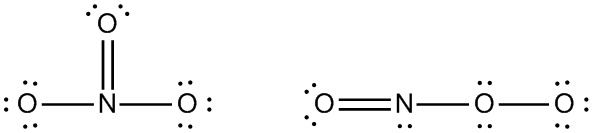
형식 전하만 고려하면,
형식 전하를 가진 원자의 개수가 더 작은
2번째 직선형 구조가 더 안정한 구조이다.
그러나,
1번째 구조는 3개의 공명 구조를 갖고 있다.
( 2번째 구조는 공명 구조가 없음. )
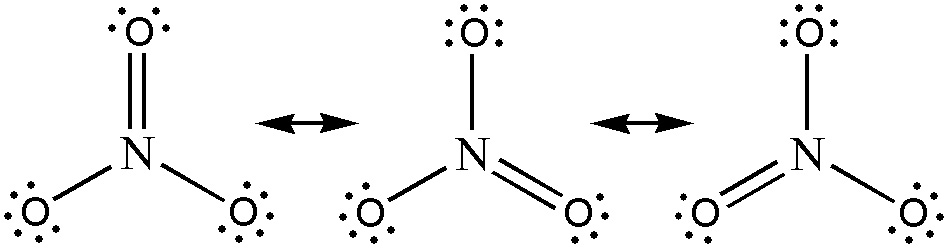
일반적으로 공명에 의한 안정 효과가
형식 전하에 의한 불안정 효과보다 더 크기 때문에,
질산 이온의 실제 루이스 구조는
1번째 구조와 같다.
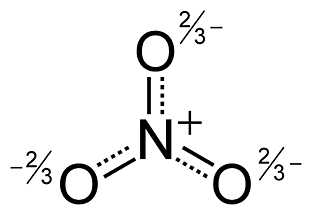
[ 그림 출처 Wikimedia ] Resonance hybrid of the nitrate ion, NO3^-.
[키워드] 질산 이온의 루이스 구조 기준, NO3^- 루이스 기준, NO3^- 루이스 구조 기준, 최대 결합수 기준
'일반화학 > [08장] 화학결합의 기본 개념' 카테고리의 다른 글
| N2O 루이스 구조 그리기 (1) | 2017.06.16 |
|---|---|
| 결합 에너지. 결합 엔탈피 ★ (0) | 2017.05.21 |
| CaCl의 격자에너지. 생성엔탈피 계산 ★ (1) | 2017.04.28 |
| 화학결합의 크기. 화학결합의 세기 ★ (1) | 2017.04.15 |
| 포름알데히드, CH2O 루이스 구조 그리기 (0) | 2017.02.12 |
| 루이스 구조(Lewis structure) 그리기 ★ (2) | 2016.11.24 |
| O2 루이스. 산소 분자의 루이스 구조식 (0) | 2016.10.24 |
| 배위결합 조건. 배위공유결합 조건. NH3–BF3 (0) | 2016.10.16 |

댓글