몰분율. mole fraction
▶ 몰분율
> “어떤 성분의 몰수와 전체 성분의 총 몰수와의 비”를 말한다.
> 몰분율 = 어떤 성분의 몰수 / 전체 성분의 총 몰수

만약 A 성분과 B 성분만으로 이루어진 2성분 용액이라면,

> X_A = n_A / (n_A + n_B)
> X_A = n_A / n_total
> X_A + X_B = 1
> X_B = 1 – X_A
▶ 몰분율은 다른 농도와 달리 “단위가 없음”에 주의할 것.
▶ 기용체(기체 용액)에만 주로 사용.
▶ 액체 용액에선 잘 사용안함.
[참고] A의 mol% = A의 몰분율 × 100

[몰분율 개념이 쉽게 이해되지 않는 학생들을 위한 자료]
과일 바구니에 사과 5개, 배 7개, 참외 8개가 있다.
과일 중에서 사과의 “개분율”은?

---------------------------------------------------
예제) 몰랄농도가 1.22 m 인 설탕 수용액에서,
설탕의 몰분율을 구하시오.
풀이) 설탕과 물로 이루어진 2성분 용액이다.
몰랄농도의 정의로부터

= 1.22 mol 설탕 / 1 kg 물
---> 용질인 설탕의 몰수는 1.22 mol 이다.
용매인 1 kg 물의 몰수를 구하면,

전체 몰수는
1.22 mol + 55.5 mol = 56.72 mol
따라서 설탕의 몰분율은

용질의 몰분율 = 용질의 몰수 / (용질의 몰수 + 용매의 몰수)
= 용액의 몰분율
[ 관련 예제 https://ywpop.tistory.com/22489 ] 23.8% w/w LiCl 용액의 몰분율
[ 관련 예제 https://ywpop.tistory.com/20207 ] 6.8 wt% 에탄올 수용액의 몰분율
[ 관련 글 https://ywpop.tistory.com/48 ] 돌턴의 분압법칙
[키워드] 몰분율 기준, 몰분율 사전
'화학 > 용액의 농도' 카테고리의 다른 글
| 40% w/w 염산(HCl) 용액(d 1.198)의 몰농도(M) (0) | 2014.11.19 |
|---|---|
| 같은 질량의 글리세롤(C3H8O3)과 물을 포함하는 용액의 농도 (0) | 2014.10.09 |
| 98% 황산 용액의 몰농도 (d 1.84) ★ (4) | 2014.10.04 |
| 몰농도(molarity, M), 몰랄농도(molality, m) ★ (8) | 2014.07.07 |
| 백만분율(ppm), 십억분율(ppb) ★ (6) | 2014.07.03 |
| 질량 백분율 (퍼센트 농도) ★ (2) | 2014.07.03 |
| 몰농도(M) 몰랄농도(m) 환산(변환) ★ (0) | 2012.09.11 |
| 몰농도 사용할 때 문제점 (2) | 2012.06.21 |
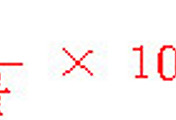



댓글