728x170
물 분자의 기하구조
---------------------------------------------------
중심 원자인 산소 원자(O) 주위에는
결합 전자쌍이 2개,
비결합 전자쌍이 2개,
총 4개 전자쌍이 있다.
4개 전자쌍 간의 반발이
가장 최소인 기하구조는 사면체이므로,
각각의 전자쌍은 사면체의 꼭지점에 각각 자리잡는다.
---> 사면체의 꼭지점에 위치하고 있을 때,
각 전자쌍은 최대로 멀리 떨어져 있다.
( 참고: VSEPR https://ywpop.tistory.com/2569 )
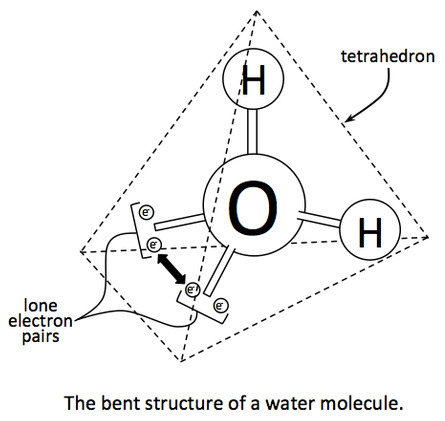
이 때문에
아래와 같은 선형 구조는 불가능하다.
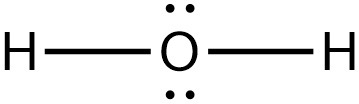
[ 관련 글 https://ywpop.tistory.com/15733 ] 분자의 기하구조를 알기 위해서는. CH4 NH3 H2O
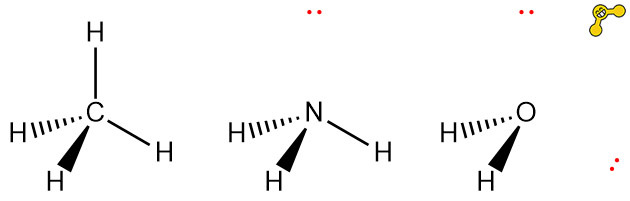
[ 관련 글 https://ywpop.tistory.com/10582 ] 물 분자. H2O molecule
[키워드] 물 분자의 기하 구조 기준문서, H2O 루이스 기준문서
반응형
그리드형(광고전용)
'일반화학 > [09장] 분자의 기하구조와 결합 이론' 카테고리의 다른 글
| H2SO4 루이스 구조 그리기 (1) | 2023.04.25 |
|---|---|
| CH3^+ 이온의 혼성 오비탈 (2) | 2023.03.20 |
| CH3O^- 루이스 구조와 형식 전하 (0) | 2023.03.19 |
| 인산의 혼성 오비탈. 인의 혼성 오비탈 (1) | 2023.03.09 |
| 전자쌍 반발 원리로 예측한 분자나 이온의 모양 (0) | 2023.02.16 |
| 전기장의 영향을 받아 일정한 방향으로 배열되는 분자 (0) | 2023.02.16 |
| dipole moment CH3Cl CH2Cl2 CHCl3 CCl4 dipole moment (0) | 2023.01.29 |
| NO, 일산화질소 극성 무극성 (0) | 2023.01.16 |



댓글