BF4^- 루이스 구조 그리기
Lewis structure of BF4^-
---------------------------------------------------
▶ 참고: 루이스 구조 그리기
[ https://ywpop.tistory.com/6302 ]
---------------------------------------------------
[1단계] 각 원자의 원자가전자 수의 합을 구한다.
(B) + 4(F) + 1 = (3) + 4(7) + 1 = 32
[2단계] 화합물의 기본 골격 구조를 그린다.
( 단일결합 수만큼 전자 수를 뺀다. )

32 – 4(2) = 24
[3단계] 주위 원자들이 팔전자 규칙에 맞도록 전자를 한 쌍씩 그린다.
( 무조건, 그냥 주위 원자 주변에 전자쌍 3개씩 그린다. )
( 그린 전자 수만큼 뺀다. )
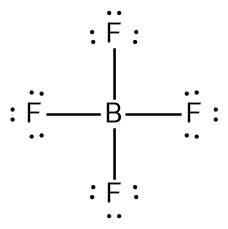
24 – 4(6) = 0
[4단계] 중심 원자도 팔전자 규칙에 맞도록 그린다.
---> 팔전자 규칙을 만족한다.

▶ 형식전하 = 원자가전자수 – 비결합전자수 – (결합전자수/2)
( 참고: 형식전하 https://ywpop.tistory.com/2544 )
> B의 형식전하 = 3 – 0 – (8/2) = –1
> F(6)의 형식전하 = 7 – 6 – (2/2) = 0
( 괄호 안 숫자는 비결합전자수. )
> 모든 원자가 옥텟규칙을 만족하고,
B의 형식전하 = –1 = 이온 전하.
---> 안정한 루이스 구조. 끝.
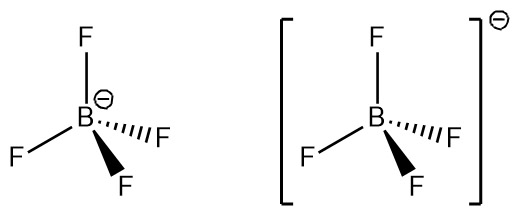
[그림] BF4^-의 기하 구조.
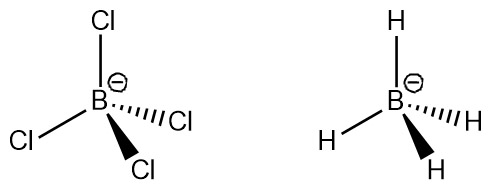
[그림] BCl4^-의 기하 구조와 BH4^-의 기하 구조.
[키워드] BX4^- 루이스, BCl4^- 루이스, BH4^- 루이스
'일반화학 > [09장] 분자의 기하구조와 결합 이론' 카테고리의 다른 글
| N2O4 루이스 구조 (1) | 2022.10.22 |
|---|---|
| CH2F2 루이스 구조. CH2F2 기하 구조 (0) | 2022.10.20 |
| NH3 루이스 구조. NH3 전자-점 구조 (0) | 2022.10.05 |
| 동핵 이원자 분자는 무극성 (0) | 2022.10.02 |
| PHCl2 루이스 구조 그리기 (0) | 2022.09.24 |
| ClO2^- 루이스 구조 그리기 (0) | 2022.09.15 |
| 분자의 화학식으로부터 분자의 기하구조 예측 (1) | 2022.09.07 |
| VSEPR. 메탄올의 결합각 (0) | 2022.09.07 |




댓글