연수기. 양이온 교환수지
1. 연수기
양이온 교환수지를 사용하여
경수(센물)를 연수(단물)로 만드는 장치로,
경수연화장치라고도 한다.
경수를 Na-형 양이온 교환수지가 들어있는 연수기에 통과시키면
물속에 존재하는 경도 성분인 칼슘 이온과 마그네슘 이온이
수지 중의 나트륨 이온과 교환된다.
따라서 연수기 출구에서는 경도 성분이 제거된 연수가 배출된다.
산업 현장에서는 주로 증기를 생산하는 수관식 보일러에
연수를 공급하기 위해 연수기를 사용한다.
물속에 경도 성분이 있으면,
파이프를 좁게 만들거나 아예 막아버리는 등의 문제를 일으키는
관석(스케일)이 잘 형성되기 때문이다.

[ 그림 출처 Wikimedia ] Boiler scale.
2. 연수기(양이온 교환)의 화학적 원리
1) 교환에 관여하는
① 양이온의 농도 비,
② 양이온과 음이온 교환기의 성질,
③ 수용액의 pH 및 공존하는 양이온의 종류
등에 의해 교환 반응의 평형 상태가 결정된다.
2) 종류에 따라 그 정도의 차이는 있지만,
양이온에 대한 양이온 교환수지의 선택성은 다음 순서로 증가한다.

4) 양이온 교환수지의 Na 성분이
통과시킨 물속의 경도 성분과 대부분 교환되면,
더 이상 연수가 만들어지지 않는다.
이때 연수기에 진한 소금(NaCl) 용액을 통과시키면
양이온 교환수지에 흡착된 경도 성분이 역으로 Na 성분과 교환되며,
그 결과 양이온 교환수지가 활성화(재생)되어
연수를 다시 제조할 수 있다.
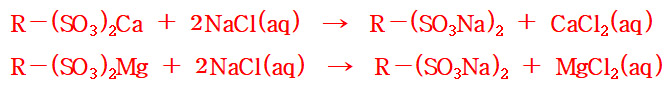
[키워드] 연수기 기준문서, 양이온 교환 수지 기준문서, 수관식 보일러 기준문서, 연수기 사전, 양이온 교환 수지 사전
'화학' 카테고리의 다른 글
| 0.600 M NH3와 0.220 mol NH4Cl 완충용액의 pH (1) | 2017.06.25 |
|---|---|
| 온도변환. 온도환산. 섭씨온도, 화씨온도, 절대온도 (0) | 2017.06.24 |
| 약염기-강산 적정. 0.600 M NH3 + HCl. 중화점 pH (0) | 2017.06.24 |
| C=0.01 M, pH=9 일 때, α(이온화도) 값? (0) | 2017.06.24 |
| 37% HCl 시약으로 3 mM HCl 용액 만들기 (0) | 2017.06.23 |
| 0.5 N NaOH 용액 400 mL 만들기 (0) | 2017.06.23 |
| 할로겐 이온과 질산은의 반응 (1) | 2017.06.23 |
| FeSO4 용액의 질량백분율, 몰농도, 몰랄농도 (3) | 2017.06.22 |
댓글