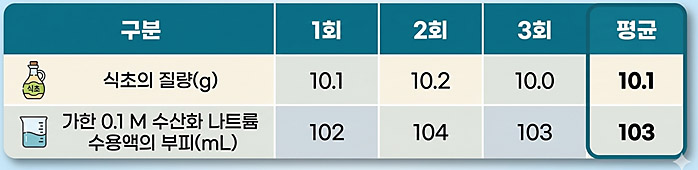
식초 10.1 g 적정에 0.1 M NaOH(aq) 103 mL 소비
------------------------
[참고] 식초 정량분석
[ https://ywpop.tistory.com/471887 ]
적정에 소비된 NaOH의 몰수를 계산하면,
n = M × V
( 참고 https://ywpop.tistory.com/7787 )
= (0.1 mol/L) (103/1000 L)
= (0.1) (103/1000)
= 0.0103 mol
산-염기 중화 반응식
CH3COOH + NaOH → CH3COONa + H2O
CH3COOH : NaOH = 1 : 1 계수비(= 몰수비) 이므로,
즉 CH3COOH : NaOH = 1 : 1 반응하므로,
적정에 소비된 NaOH의 몰수
= 식초에 들어있는 CH3COOH의 몰수
= 0.0103 mol
CH3COOH의 몰질량 = 60 g/mol 이므로,
0.0103 mol CH3COOH의 질량을 계산하면,
W = n × M
( 참고 https://ywpop.tistory.com/7738 )
= 0.0103 mol × (60 g/mol)
= 0.618 g
식초에 들어있는 CH3COOH의 함량(%)을 계산하면,
(CH3COOH의 질량 / 식초의 질량) × 100
= (0.618 g / 10.1 g) × 100
= 6.1188%
답: 6.12%
[참고] 아세트산의 몰농도
“식초 = 아세트산 수용액” 이므로,
식초의 밀도 = 1 g/mL 라 가정하면,
식초의 부피 = 10.1 mL
= 아세트산 수용액의 부피
아세트산의 몰농도
= 용질 mol수 / 용액 L수
= 0.0103 mol / (10.1/1000 L)
= 1.0198 mol/L
≒ 1.02 M
[ 관련 글 https://ywpop.tistory.com/7176 ]
7.63% 식초의 몰농도
= 0.00385 mol / (3.00/1000 L)
= 1.2833 mol/L
≒ 1.28 M
[ 관련 글 https://ywpop.tistory.com/11316 ]
8.4657 g 식초 정량분석. 0.1 N NaOH (f 1.0451) 14.5 mL 소비
---> 식초를 묽힌 후(희석시켜) 정량분석. 일반적인 실험방법
[ 관련 글 https://ywpop.tistory.com/10993 ]
식초를 희석시켜 사용하는 이유
[키워드] 식초 정량분석 기준, 아세트산 정량분석 기준, 식초 정량분석 사전, 아세트산 정량분석 사전
'화학' 카테고리의 다른 글
| 25 mL 식초 100 mL 희석. 25 mL + 0.2 M NaOH 25 mL (9) | 2025.11.20 |
|---|---|
| 10 mL 식초 100 mL 희석. 25 mL + 0.1 M NaOH 20 mL ★ (6) | 2025.11.18 |
| [아스피린 합성 실험] 아세트산 무수물 취급 시 주의할 점 (10) | 2025.11.11 |
| 미생물의 농도와 시간. C = a exp(-bt) (1) | 2025.10.23 |
| 아스피린 합성. 살리실산 4 g + 아세트산무수물 6 mL (3) | 2025.08.28 |
| LNG의 성질에 대한 설명 중 틀린 것 (3) | 2025.05.02 |
| 저울로 시료를 칭량할 때 적은 양과 많은 양의 오차 정도 (2) | 2024.11.18 |
| 과탄산소다. 과탄산 소듐. sodium percarbonate (1) | 2024.11.13 |


댓글