수소 모자람 지수. IHD. 불포화도
수소 모자람 지수 (Index of Hydrogen Deficiency, IHD) 는
분자식으로부터 이중 결합, 고리형, 삼중 결합의 개수를
결정할 수 있는 방법을 제공하기 때문에,
미지시료의 구조를 분석할 때 상당히 유용한 개념이다.
[ IHD 계산식 순서 ]
예제 1) C7 H14 O2
1) 분자식에 있는 탄소 개수로 비고리형 포화탄화수소 식을 구한다.
⇨ C7 H16
from

2) 5A족 원소(N, P)가 있으면,
그 개수만큼 수소 개수를 더한 다음,
5A족 원소를 분자식에 추가한다.
⇨ C7 H16
3) 6A족 원소(O, S)가 있으면,
그냥 6A족 원소를 분자식에 추가한다.
⇨ C7 H16 O2
4) 할로겐족 원소가 있으면,
그 개수만큼 수소 개수를 뺀 다음,
할로겐족 원소를 분자식에 추가한다.
⇨ C7 H16 O2 (IHD 계산식 종료)
5) IHD 계산식과 시료의 분자식에 나와 있는
수소 개수 차이를 2로 나눈 값이 수소 모자람 지수가 된다.
> IHD 계산식: C7 H16 O2
> 시료의 분자식: C7 H14 O2
Δ(#H) / 2 = 2 / 2 = 1 = IHD
IHD 1은 분자 내에 이중 결합 1개 또는 고리 1개가 존재한다는 것을 알려준다.
만약 이중 결합이라면, C=C 또는 C=O 이중 결합을 의심해 볼 수 있으며,
C=O 이중 결합은 적외선(IR) 스펙트럼만으로도 쉽게 확인이 가능하다.
예제 1)의 분자는 isopentyl acetate(isoamyl acetate)이다.


[1744 cm-1, C=O str. peak]
예제 2) C10 H14 N2
1) C10 ⇨ C10 H22
2) N2 ⇨ C10 H24 N2
5) IHD = (24–14) / 2 = 5
---> (다중 결합 and/or 고리) 5개.
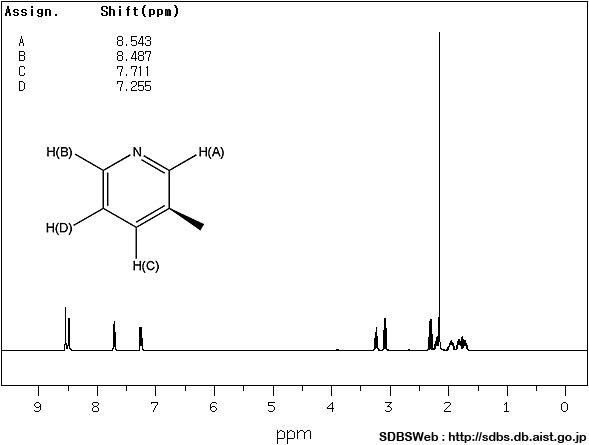
IHD가 4 이상이면, 벤젠 고리를 포함하고 있을 가능성이 높으며,
이것은 NMR로 쉽게 확인이 가능하다.
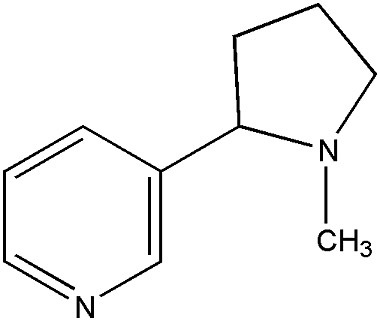
예제 2)의 분자는 니코틴(nicotine)이다.
IHD 5는 이중 결합 3개, 고리 2개와 일치한다.
[ IHD 계산 공식 ]
IHD = (2C + 2 – H + N – X) / 2
또는
IHD = C + 1 – (H – N + X)/2
> C = 탄소 원자의 개수
> H = 수소 원자의 개수
> N = 질소 원자의 개수
> X = 할로겐 원자의 개수
예제 3) C7 H14 O2
IHD = C + 1 – (H – N + X)/2
= 7 + 1 – (14 – 0 + 0)/2 = 1
예제 4) C10 H14 N2
IHD = 10 + 1 – (14 – 2 + 0)/2 = 5
[참고] 유기화학 불포화도 degree of unsaturation
= index of hydrogen deficiency
= double bond equivalents
= unsaturation index
[ 관련 예제 https://ywpop.tistory.com/6719 ] C4H9N의 IHD 계산
[키워드] 수소 모자람 지수 기준, 수소 결핍 지수 기준, IHD 기준, 불포화도 기준, 수소 모자람 지수 사전, 수소 결핍 지수 사전, IHD dic, 불포화도 사전
'분광학' 카테고리의 다른 글
| 자외선(UV-Visible) 분광법에서 용매 선택(효과) (1) | 2014.12.19 |
|---|---|
| 레이저(Laser)의 특징 (0) | 2014.11.29 |
| Shielding vs. Deshielding: H-NMR of nitrile(cyano-) and acetylene(ethyne) (0) | 2014.11.20 |
| NMR 기초 원리: NMR과 초전도체 (1) | 2014.11.01 |
| NMR에서 화학적 동등성과 자기적 동등성(1) (3) | 2014.08.27 |
| 2015학년도 MEET 자연과학2(의학) 28번 문제 해설 (0) | 2014.08.25 |
| 질량 분석법. Mass Spectrometry (MS) (0) | 2014.08.12 |
| Nanoparticles. 나노입자 (0) | 2014.06.25 |



댓글