구리와 아연의 전자배치. Cu와 Zn의 전자배치
고등학교 수준에서는 이해하기 어려울 수도 있습니다.
배치순서(규칙)에 따른 Cu의 바닥상태 전자배치는
[Ar] 4s^2 3d^9인데,
d^9 보다는 d^10 전자배치가 더 안정하기 때문에,
( 이유는 고등학교 수준에서 설명 불가 )
실제 Cu는 [Ar] 4s^1 3d^10과 같은 전자배치를 갖습니다.
( 참고: Cr Cu 전자배치 https://ywpop.tistory.com/2844 )
이런 속사정(?)이 있기에,
Cu가 이온화될 때는
4s^1 3d^10 전자배치에 의한 Cu^+ 이온,
4s^2 3d^9 전자배치에 의한 Cu^2+ 이온 (Cu의 주요 이온전하, 산화수),
( 참고: Cu^2+ 이온 https://ywpop.tistory.com/22090 )
이후 전이금속의 특성에 의한 Cu^3+ 이온이 될 수 있습니다.
( 참고: 전이금속 https://ywpop.tistory.com/7346 )
Zn의 경우,
실제 바닥상태 전자배치가 [Ar] 4s^2 3d^10이고,
3d 오비탈은 처음부터 전부 전자로 채워져 있기 때문에,
3d 전자는 원자가전자가 아닌 핵심부전자에 속합니다.
즉, Zn의 원자가전자는 4s^2 이므로,
Zn이 이온화될 때는 Zn^2+ 이온만 됩니다.
( 참고: 로마숫자 https://ywpop.tistory.com/8904 )
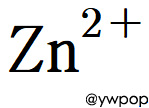
이 때문에 일부 학자들은
아연을 전이금속으로 취급하지 않기도 합니다.
[키워드] 아연의 원자가전자 기준, 아연의 바닥상태 전자배치 기준, 아연의 전자배치 기준, 아연의 이온전하 기준, 아연의 산화수 기준, 아연은 전이금속 기준, 아연 이온 기준, 아연 이온 사전, 구리 이온 기준, 구리 이온 사전, 아연은 전이금속 사전, 아연은 전이금속 제외 기준, 아연은 전이금속 제외 사전, Cu의 전자배치 기준, Zn의 전자배치 기준, Cu의 전자배치 사전, Zn의 전자배치 사전, 아연의 이온전하 기준, Zn의 이온전하 기준, 아연의 이온전하 사전, Zn의 이온전하 사전
'일반화학 > [23장] 전이 금속과 배위 화학' 카테고리의 다른 글
| [예제] 배위화합물 명명법. 착물 명명법 (0) | 2020.07.29 |
|---|---|
| [착물 명명법] Rules for Naming Complexes (0) | 2020.03.04 |
| [착물 명명법] bromopentacyanocobaltate(III) ion (0) | 2020.03.03 |
| 착이온 [Fe(CN)6]^3- 에 대한 설명 (2) | 2019.10.29 |
| 고스핀 착물과 저스핀 착물. 저스핀 착물과 고스핀 착물 (2) | 2019.08.14 |
| 헤모글로빈. hemoglobin (0) | 2019.07.24 |
| 킬레이트 효과. chelating effect (1) | 2019.07.04 |
| 정팔면체 착물. MA4B2 이성질체, MA4B2 isomer (0) | 2019.06.05 |



댓글