[Co(H2O)6]^3+의 3d 오비탈에서 홀전자 수
[Co(H2O)6]^3+는 저스핀 착물
▶ Co의 전자 배치와 Co^3+의 전자 배치
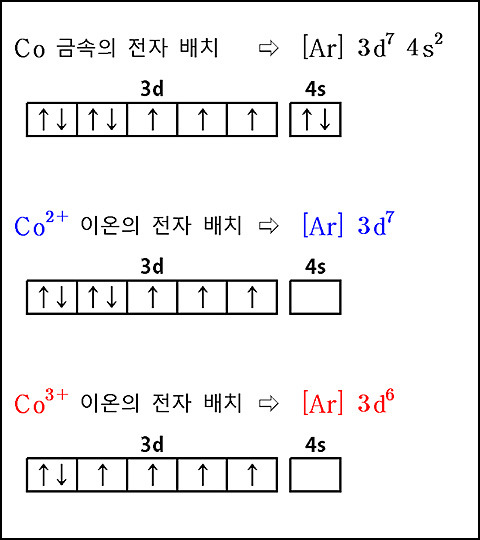
▶ H2O는 약한 장 리간드이므로,
( 참고 https://ywpop.tistory.com/4410 )
[Co(H2O)6]^3+는
고스핀 착물 (high spin complex)을 형성할 것으로 예상된다.
▶ 그러나
[Co(H2O)6]^3+는 저스핀 착물 (low spin complex)을 형성한다.
> 금속 이온의 이온 전하(= 산화수)가 증가할수록,
금속-리간드 상호작용은 증가한다.
( ∵ 금속-리간드 상호작용의 본질은 정전기적 인력 )
> Co^3+는 Ni^3+ 다음으로
주기율표에서 가장 오른쪽에 위치하고 있기 때문에,
유효 핵전하도 강해서,
다른 금속 이온보다 더 강하게 리간드를 끌어당긴다.
> 이 때문에
비록 H2O가 약한 장 리간드이지만,
[Co(H2O)6]^3+는 저스핀 착물을 형성한다.
> Almost all Co^3+ (d^6) complexes are low spin,
including [Co(H2O)6]^3+, except [CoF6]^3-, which is high spin.
▶ d^6의 전자배치
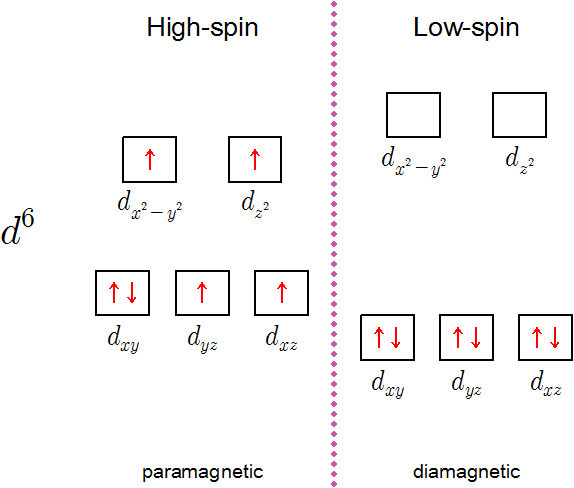
( 참고 https://ywpop.tistory.com/2909 )
---> low spin complex의 홀전자 수 = 0개
답: [Co(H2O)6]^3+의 3d 오비탈에서 홀전자 수 = 0개
[참고] 몇 가지 착물의 스핀 상태.

[키워드] [Co(H2O)6]^3+ 기준, [Co(H2O)6]^3+ dic, [Cr(H2O)6]^2+ 기준, [Fe(H2O)6]^3+ 기준, [Fe(H2O)6]^2+ 기준, [Fe(CN)6]^4- 기준, [CoF6]^3- 기준, [Co(NH3)6]^3+ 기준, [Co(H2O)6]^2+ 기준, [Co(H2O)6]^3+ 착 이온 기준, [Co(H2O)6]^3+ 착 이온 dic, [Cr(H2O)6]^2+ 착 이온 기준, [Fe(H2O)6]^3+ 착 이온 기준, [Fe(H2O)6]^2+ 착 이온 기준, [Fe(CN)6]^4- 착 이온 기준, [CoF6]^3- 착 이온 기준, [Co(NH3)6]^3+ 착 이온 기준, [Co(H2O)6]^2+ 착 이온 기준, Co 착물 기준, 코발트 착물 기준, Co 착이온 기준, 코발트 착이온 기준, Co 착물 사전, 코발트 착물 사전, Co 착이온 사전, 코발트 착이온 사전, Co(H2O)6^3+ 기준, Co(H2O)6^3+ dic, Cr(H2O)6^2+ 기준, Fe(H2O)6^3+ 기준, Fe(H2O)6^2+ 기준, Fe(CN)6^4- 기준, CoF6^3- 기준, Co(NH3)6^3+ 기준, Co(H2O)6^2+ 기준, Co(H2O)6^3+ 착 이온 기준, Co(H2O)6^3+ 착 이온 dic, Cr(H2O)6^2+ 착 이온 기준, Fe(H2O)6^3+ 착 이온 기준, Fe(H2O)6^2+ 착 이온 기준, Fe(CN)6^4- 착 이온 기준, CoF6^3- 착 이온 기준, Co(NH3)6^3+ 착 이온 기준, Co(H2O)6^2+ 착 이온 기준
[FAQ] [①22/12/17]
'일반화학 > [23장] 전이 금속과 배위 화학' 카테고리의 다른 글
| 구리가 +2가 양이온인 이유 (1) | 2022.08.23 |
|---|---|
| [Fe(H2O)6]^2+ 착이온의 전자배치와 자기적 성질 (0) | 2022.08.22 |
| [Fe(CN)6]^4- 착이온의 전자배치와 자기적 성질 (1) | 2022.08.22 |
| Sc-Zn 전이금속 +2가 전자배치 4개 홀전자 (0) | 2022.06.14 |
| 착염에 해당하는 것. K4Fe(CN)6 (0) | 2022.01.21 |
| porphine. 네 자리 리간드 (4) | 2022.01.12 |
| salen. 네 자리 리간드 (0) | 2022.01.12 |
| diethylenetriamine. 세 자리 리간드 (0) | 2022.01.12 |


댓글