이온결합 화합물의 용해도 지침, solubility guidelines
> 가용성염과 난용성염(불용성염), 수용성염과 앙금(침전물)
---------------------------------------------------
▶ 참고: 가용성염, 난용성염(앙금) 설명
[ https://ywpop.tistory.com/6892 ]
▶ 참고: 앙금 생성 반응은 교환(복분해) 반응
[ https://ywpop.tistory.com/3364 ]
---------------------------------------------------
어떤 이온결합 화합물이 물에 잘 용해될지, 안될지를 설명할 수 있는
이론, 법칙, 또는 수식은 없다.
즉, 왜 NaCl은 물에 잘 용해되고, 왜 AgCl은 물에 거의 용해되지 않는지,
이유를 설명할 수 있는 이론은 없다는 것이다.
“경험상 어떤 물질은 물에 잘 용해된다고 판단할뿐,
용해도에 관한 일반적인 법칙은 존재하지 않는다.”
[참고] 그래도 뭔 설명이라도 해보라고 하면,
난용성염은 ‘용질-용질’간 힘이 ‘용질-용매’간 힘보다 더 강하기 때문에,
( 앙금들끼리 인력 > 앙금-물 사이의 인력 )
난용성염은 물에 거의 용해되지 않는다고 설명할 수 있다.
( 관련 글 https://ywpop.tistory.com/10183 )
( 관련 글 https://ywpop.tistory.com/11781 )
다만, 다음 표와 같은 간단한 ‘용해도 지침(guidelines)’만 있을 뿐이다.
( 아래 표만 외워도 앙금 생성 관련 문제는 대부분 해결할 수 있다. )
( 만약 아래 표가 어떤 이론으로 설명가능하다면,
즉 아래 표의 결과를 설명할 수 있는 어떤 이론이 있다면,
용해도 지침이 아닌, ‘용해도 법칙 또는 용해도 규칙’이라 부를 것이다. )
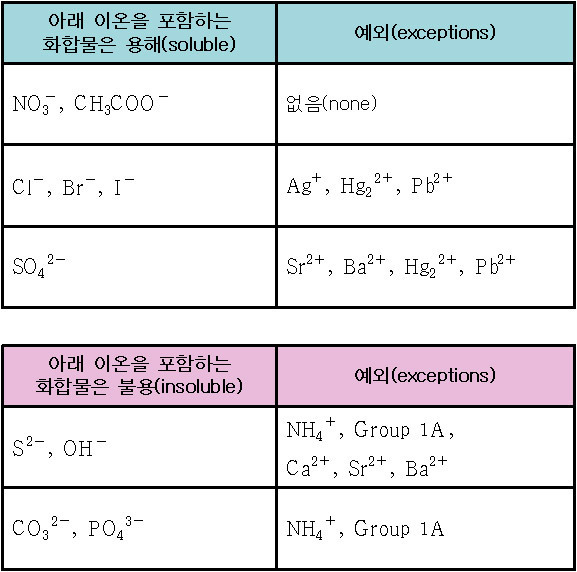
[참고] Group 1A: Li^+, Na^+, K^+, Rb^+, Cs^+
[추가] CrO4^2- 이온을 포함하는 화합물은 난용(insoluble)
> 예외: Na2CrO4, K2CrO4, (NH4)2CrO4, MgCrO4, CaCrO4, Al2(CrO4)3, NiCrO4
[추가] CaSO4는 난용성염. CaSO4의 Ksp = 4.93×10^(-5)
[참고] Ca(OH)2의 용해도는 다른 강염기에 비해 상당히 낮기 때문에,
난용성염으로 분류하는 경우도 있음.
> Ca(OH)2의 Ksp = 5.5×10^(-6)
( 참고: 강염기의 종류 https://ywpop.tistory.com/10085 )
[참고] Ag2SO4(s): slightly soluble
▶ 참고: 용해도 지침 표 사용 방법
[ https://ywpop.tistory.com/9006 ]
[예1] NaCl은 가용, AgCl은 난용. Na2SO4는 가용, BaSO4는 난용.
[예2] Al(OH)3는 난용, NaOH는 가용. BaCO3는 난용, K2CO3는 가용.
정리하면,
어떤 음이온을 포함하는 염은 대부분 물에 잘 용해되는데,
예외적으로 몇몇 양이온과 만나면, 물에 잘 용해되지 않더라.
어떤 음이온을 포함하는 염은 대부분 물에 잘 용해되지 않는데,
예외적으로 몇몇 양이온과 만나면, 물에 잘 용해되더라.
위 표는 단순무식하게 모든 종류의 이온 화합물을
하나씩, 일일이, 물에 용해시켜 봐서,
용해되는 것과 안 되는 것을 정리한 결과물에 지나지 않는다.
초등학생도 실험을 통해 만들 수 있는 도표인지라,
명칭도 용해도 지침(guidelines)이라고 붙였다.
용해도 규칙(rules)이라고 표기하는 교재도 있지만,
규칙이라고 할 수 없을 정도로 예외가 많다.
( 무엇보다 규칙이라면, 이 규칙을 뒷받침해줄 이론이 있어야 하는데,
이론이 없기 때문에, 규칙이라고 하지 않는다. )
따라서 어떤 이온 화합물이 물에 잘 용해되는지를
모두 암기하는 것은 불가능하기 때문에,
위와 같이 많이 쓰이는 몇 가지 이온 화합물의 용해도 특성만
이해하면 좋을 것 같다.
나머지 이온 화합물의 용해도 특성은 다음 링크 자료에서 조회가 가능하다.
[ Solubility chart ]
[ Solubility table ]
[ 관련 예제 https://ywpop.tistory.com/search/침전반응 ] “알짜”와 “침전반응” 키워드를 둘 다 포함하는 제목
[ 관련 예제 https://ywpop.tistory.com/13568 ] 앙금(침전) 예측. ZnSO4 Mn(OH)2 AgClO3 CaCO3 AgCl
[키워드] 침전 반응 기준문서, 앙금 기준문서, 용해도 지침 사전, 앙금 사전
AgNO3(aq) + CH3COONa(aq) → CH3COOAg(s)↓ + NaNO3(aq) : 단, 진한 농도에서.
( 참고 https://en.wikipedia.org/wiki/Silver_acetate )
---------------------------------------------------
Colors of some common water-insoluble salts (precipitates)

> Cadmium sulfide, CdS is a yellow solid.

[그림] AgCl, PbCl2, Hg2Cl2는 흰색 침전.
'일반화학 > [04장] 수용액 반응' 카테고리의 다른 글
| 산소의 득실과 산화-환원 반응의 동시성 (0) | 2014.11.25 |
|---|---|
| 화학 반응에서 염(salt)이란 (0) | 2014.11.13 |
| 산화-환원 반응에서 불균등화 반응 ★ (0) | 2014.11.08 |
| 매우 묽은 농도의 강산 강염기 용액의 pH (1) | 2014.11.05 |
| 0.10 M HNO3 500 mL + 0.10 M Ca(OH)2 500 mL 혼합 용액의 pH (0) | 2014.10.18 |
| 용액의 묽힘(희석, dilution) 법칙(원리) ★ (10) | 2014.10.07 |
| 산화수 구하는 규칙(rule) ★★ (14) | 2014.07.30 |
| 산과 염기의 정의. definition of acid and base ★ (8) | 2014.07.21 |




댓글