Sulfur Tetrafluoride(SF4) 분자의 Seesaw Molecular Geometry 설명
Sulfur Tetrafluoride (사플루오린화 황) 분자의 중심 원자는 황(S)이고,
황의 전자 영역은 5개(단일 결합 4개 + 비결합전자쌍 1개)이므로,
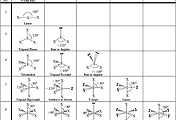
Sulfur Tetrafluoride 분자의 기본 기하 구조는 삼각이중피라미드(Trigonal Bipyramidal)이다.
중심 원자가 sp^3d 혼성 오비탈이므로,
( 참고 https://ywpop.tistory.com/7475 )
전자 영역의 기하 구조는 trigonal bipyramidal.
( 참고 https://ywpop.tistory.com/11542 )
그러나 황 원자에 존재하는 비결합전자쌍 1개 때문에,
Sulfur Tetrafluoride 분자는 삼각이중피라미드 구조가 아닐 것으로 예측된다.
황 원자의 5개 전자 영역 중에서, 비결합전자쌍 1개는 어느 곳에 위치할까?
비결합전자쌍(Lone pair)과 90° 위치에서 반발하는 결합전자쌍만 체크해 보자.
(∵ 120° 정도 떨어져 있는 전자쌍 간 반발력은 90° 위치에 비해 상대적으로 약하기 때문에 무시하자.)
> Lone pair가 축 위치에 있을 경우, 반발 가능한 전자쌍은 3개.
> Lone pair가 평면 위치에 있을 경우, 반발 가능한 전자쌍은 2개.
∴ Lone pair가 평면 위치에 있을 경우, 전자쌍 간 반발이 최소가 된다.
[ SF4 루이스 구조 그리기 설명 https://ywpop.tistory.com/9976 ]
▶ red S-F 결합전자쌍은 비결합전자쌍과 90° 위치에서 강하게 반발한다.
---> red S-F 결합전자쌍은 비결합전자쌍에서 최대한 멀리 떨어져 있으려 한다.
---> 이 때문에, F-S-F 결합각과 S-F 결합길이, 둘 다 증가한다.
> red S-F bond length = 164.6 pm
> blue S-F bond length = 154.5 pm
▶ SF4는 극성. SF4 is polar.
( 참고 https://www.quora.com/Is-SF4-consided-polar-or-nonpolar )
[ 관련 글 https://ywpop.tistory.com/2576 ] ClF3 분자의 T-shaped Molecular Geometry 설명
[키워드] SF4 기준문서, SF4 루이스, SF4 기하구조, SF4 polar or nonpolar, SeF4 기준문서, SeF4 루이스, SeF4 기하구조, SeF4 polar or nonpolar, VSEPR 기준문서, 90도 반발 기준문서
'일반화학 > [09장] 분자의 기하구조와 결합 이론' 카테고리의 다른 글
| 분자 오비탈 전자 배치. 산소 분자(O2), 이온(O2^2-) (0) | 2014.10.21 |
|---|---|
| NO2 NO2^+ NO2^- NO NO^-의 루이스 구조식 ★ (5) | 2014.09.29 |
| 혼성 오비탈 (hybrid orbital) ★ (9) | 2014.06.27 |
| 원자가 결합 이론. Valence Bond Theory, VBT (3) | 2014.06.27 |
| 원자가 껍질 전자쌍 반발 모형으로 분자의 기하 구조 예측 (3) (0) | 2014.05.29 |
| 원자가 껍질 전자쌍 반발 모형으로 분자의 기하 구조 예측 (2) (0) | 2014.05.29 |
| 원자가 껍질 전자쌍 반발 모형으로 분자의 기하 구조 예측 (1) (2) | 2014.05.28 |
| 분자의 기하 구조와 원자가 껍질 전자쌍 반발 모형 (VSEPR model) (2) | 2014.05.27 |









댓글