3대 강산(强酸). 염산, 황산, 질산
“염산 > 황산 > 질산” 순으로 더 강산입니다.
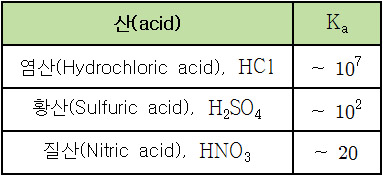
▶ 3대 강산의 이온화 반응식
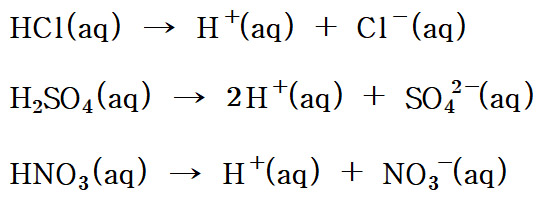
> HCl(aq) → H^+(aq) + Cl^-(aq)
> H2SO4(aq) → 2H^+(aq) + SO4^2-(aq)
> HNO3(aq) → H^+(aq) + NO3^-(aq)
( 참고: 산-염기의 정의 https://ywpop.tistory.com/2696 )
( 참고: 6대 강산 https://ywpop.tistory.com/4273 )
---------------------------------------------------
[진한 황산을 묽혀서 사용할 때 주의사항]
황산은 묽은 황산이 강한 산입니다.
시판되는 진한 황산은 황산의 질량비가 96~98% 이상의 수용액인데,
물이 거의 없기 때문에 이온화되는 황산이 거의 없어서
거의 산성을 나타내지 않습니다.
대신 탈수력이 강력해서 진한 황산 역시 매우 위험한 물질입니다.
진한 황산은 물과 만나면 급격히 이온화되는데,
이때 용액이 끓어 튈 정도로 한꺼번에 많은 열이 방출되기 때문에,
실험실에서 진한 황산과 물을 혼합하여 묽은 황산 용액을 만들 때는,
반드시 비커 등과 같은 용기에 다량의 물을 먼저 넣고
여기에다 진한 황산을 몇 방울씩 천천히 떨어뜨려 만들어야 합니다.
그 이유는 진한 황산(d 1.84)은 물보다 비중이 크기 때문에,
진한 황산 방울을 물에 떨어뜨리면
물속으로 가라앉으면서 열이 분산되므로,
황산 용액이 밖으로 튀지 않습니다.
만약 반대로 진한 황산에다 물을 떨어뜨리면
물이 황산 위에 뜬 상태에서 끓기 때문에
황산 용액이 밖으로 튈 수 있습니다.
[ 관련 글 https://ywpop.tistory.com/6158 ] 메스플라스크 사용법. 부피플라스크 사용법
[키워드] 황산의 묽힘 기준, 황산을 묽힐 때 기준, 3대 강산 기준, 3대 강산 사전
'화학' 카테고리의 다른 글
| 용액의 농도 환산: 질량 백분율, 몰농도, 몰랄농도, 몰분율 (0) | 2014.09.30 |
|---|---|
| [총괄성-어는점내림] 수용액의 어는점내림 (0) | 2014.09.30 |
| [총괄성-어는점내림] 수용액의 어는점내림 (0) | 2014.09.30 |
| 질량 백분율, 몰분율, 몰랄농도, 몰농도 계산 문제 (0) | 2014.09.26 |
| 수소 양이온 = 양성자? (0) | 2014.09.24 |
| 화학 반응식 균형 맞추기, 균형 맞춘 반응식 완성하기 (1) | 2014.09.16 |
| 자발적 과정과 열역학 제1법칙 (1) | 2014.08.13 |
| 자발적 과정과 비자발적 과정 (2) | 2014.08.13 |




댓글