40.0% C, 6.7% H, 53.3% O, mol mass 60 g/mol
40.0% C, 6.7% H, 53.3% O, mol mass 60 g/mol
A compound is 40.0% carbon, 6.7% hydrogen and 53.3% oxygen.
Determine the empirical formula and molecular formula
if actual molar mass of compound is 60 g/mol.
---------------------------------------------------
▶ 참고: 원소분석
[ https://ywpop.tistory.com/64 ]
---------------------------------------------------
각 성분의 몰수 계산
> C의 몰수 = 40.0 / 12 = 3.33 mol
> H의 몰수 = 6.7 / 1 = 6.7 mol
> O의 몰수 = 53.3 / 16 = 3.33 mol
몰수의 가장 작은 정수비 계산
C : H : O = 3.33 : 6.7 : 3.33
= 3.33/3.33 : 6.7/3.33 : 3.33/3.33
= 1 : 2.01 : 1
≒ 1 : 2 : 1
---> 실험식 = C H2 O
---> 실험식량 = (12) + 2(1) + (16) = 30
분자량 / 실험식량 = 60 / 30 = 2 = n
분자식 = n(실험식) = 2(CH2O) = C2H4O2
답: 실험식 = CH2O, 분자식 = C2H4O2
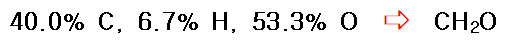
[ 관련 글 https://ywpop.tistory.com/14415 ] 40.0% C, 6.7% H, 53.3% O, mol mass 180 g/mol
[키워드] C 40.0%, H 6.7%, O 53.3% 기준문서, 40.0% C, 6.7% H, 53.3% O 기준문서