CCl2F2의 결합각도. bond angle for CCl2F2
CCl2F2의 결합각도. bond angle for CCl2F2
Dichlorodifluoromethane의 결합각도
---------------------------------------------------
중심 원자의 전자 영역 = 4 이므로,
기본적인 결합각도는 109.5도.
( 참고 https://ywpop.tistory.com/2571 )
원자의 크기가 더 큰 Cl은 F보다 더 많은 공간을 차지한다.
( 경차 뒷좌석에 강호동과 유재석이 앉아있다고 상상해봐라.
누가 더 많은 공간을 차지하고 있을까? )
이 때문에
Cl을 포함하는 결합각도는 109.5도보다 약간 더 크고,
F를 포함하는 결합각도는 109.5도보다 약간 더 작다.
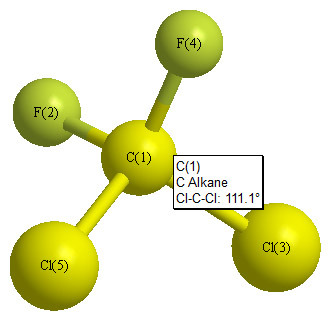
∠Cl-C-Cl = 111.1°
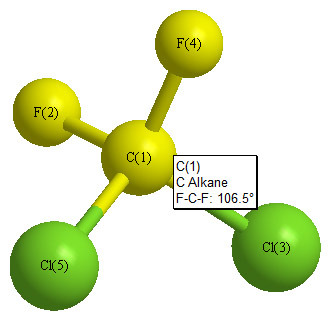
∠F-C-F = 106.5°

∠F-C-Cl = 109.8°
CF2Cl2는 극성 분자.
The C-F bonds are more polar than the C-Cl bonds.
---> CF2Cl2 is a polar molecule.
---> dipole moment, μ > 0
( 참고 https://12uchem.files.wordpress.com/2017/03/6-en-and-polarity-homework-answers.pdf )
만약 링크가 깨지면,
[키워드] R-12의 결합각도, CFC-12의 결합각도, CF2Cl2의 결합각도, CF2Cl2 polar or nonpolar